



 海外直邮
海外直邮
 药师指导
药师指导
 隐私服务
隐私服务
 签订合同
签订合同
唑来膦酸、注射用唑来膦酸、择泰、艾瑞宁、zoledronic acid、ZOMETA、1-羟基-2-(咪唑-1-基)-亚乙基-1、1-二磷酸
止痛
24个月
瑞士诺华
4毫克/100毫升、4毫克/5毫升
注射剂
通用名称:zoledronic acid
商品名称:ZOMETA、择泰
英文名称:zoledronic acid
中文名称:注射用唑来膦酸
全部名称:唑来膦酸、注射用唑来膦酸、择泰、艾瑞宁、zoledronic acid、ZOMETA、1-羟基-2-(咪唑-1-基)-亚乙基-1、1-二磷酸
1、恶性肿瘤高钙血症
唑来膦酸(择泰、ZOMETA)用于治疗恶性肿瘤的高钙血症,定义为白蛋白校正钙(cCa)大于或等于12毫克/分升[3.0mmol/升],公式为:cCa毫克/分升 = Ca毫克/分升+0.8(4.0克/分升-患者白蛋白[克/分升])。
2、多发性骨髓瘤与实体瘤骨转移
唑来膦酸(择泰、ZOMETA)适用于治疗多发性骨髓瘤患者和有记录的实体瘤骨转移的患者,并结合标准的抗肿瘤治疗。前列腺癌应该在接受至少一种激素治疗后取得进展。
使用限制:唑来膦酸(择泰、ZOMETA)治疗甲状旁腺功能亢进相关高钙血症或其他非肿瘤相关疾病的安全性和疗效尚未确定。
1、注射剂:4毫克/100毫升(0.04毫克/毫升)单剂量即用瓶装。
2、注射剂:4毫克/5毫升(0.8毫克/毫升)单剂量瓶,用于静脉注射前稀释。
在溶液和容器允许的情况下,应在给药前目视检查肠胃外药物产品是否存在颗粒物质和变色。
1、恶性肿瘤高钙血症
恶性肿瘤高钙血症[白蛋白校正的血清钙大于或等于12毫克/分升(3.0mmol/升)]中唑来膦酸(择泰、ZOMETA)滨的最大推荐剂量为4毫克。4毫克剂量必须在不少于15分钟内以单剂量静脉输注的形式给药。接受唑来膦酸(择泰、ZOMETA)治疗的患者应在每次治疗前进行血清肌酸酐评估。
对于出现轻度至中度肾功能损害的恶性肿瘤高钙血症患者,开始治疗前无需调整唑来膦酸(择泰、ZOMETA)的剂量(血清肌酸酐低于400mol/升或低于4.5毫克/分升)。
服用唑来膦酸(择泰、ZOMETA)之前,患者应充分补水。
当考虑使用唑来膦酸(择泰、ZOMETA)时,应考虑肿瘤诱导的高钙血症的严重程度和症状。作为高钙血症治疗不可或缺的一部分,应立即开始剧烈的盐水水合作用,并在整个治疗期间尝试将尿量恢复至约21/天。轻度或无症状的高钙血症可采用保守治疗(即盐水化,联合或不联合袢利尿剂)。在整个治疗过程中,患者应充分饮水,但必须避免过度饮水,尤其是对于心力衰竭患者。纠正低血容量之前不应采用利尿剂治疗。
如果血清钙在初始治疗后未恢复正常或保持正常,可考虑使用唑来膦酸(择泰、ZOMETA)4毫克进行再治疗。建议再次治疗前至少经过7天,以便对初始剂量产生完全反应。在接受佐美特治疗的所有患者中,必须仔细监测肾功能,并且在再次接受唑来膦酸(择泰、ZOMETA)治疗之前必须评估血清肌酸酐。
2、多发性骨髓瘤与实体瘤骨转移
对于肌酐清除率(CrCl)大于60毫升/分钟的多发性骨髓瘤和实体瘤转移性骨病变患者,每3至4周输注4毫克,输注时间不少于15分钟。最佳治疗时间尚不清楚。
开始治疗时,肾功能降低(轻度和中度肾功能损害)患者的唑来膦酸(择泰、ZOMETA)推荐剂量见下表。计算这些剂量是为了达到相同的面积下
曲线(AUC)为肌酐清除率为75毫升/分钟的患者中获得的曲线。肌酐清除率采用Cockcroft-Gault公式计算。
表:基线CrCl小于或等于60毫升/分钟患者的减少剂量

*假设目标AUC为0.66(mg·HR/L)(CrCl = 75毫升/分钟)计算的剂量。
在治疗期间,应在每次服用唑来膦酸(择泰、ZOMETA)之前测量血清肌酸酐,并应停止肾脏恶化治疗。在临床研究中,肾脏恶化的定义如下:
对于基线肌酐正常的患者,增加0.5毫克/分升。
对于基线肌酐异常的患者,增加1.0毫克/分升。
在临床研究中,仅当肌酐恢复至基线值的10%以内时,才恢复唑来膦酸(择泰、ZOMETA)治疗。应使用中断治疗前的相同剂量重新开始唑来膦酸(择泰、ZOMETA)。
患者还应每日口服500毫克的钙补充剂和含400国际单位维生素D的复合维生素。
3、溶液制备
唑来膦酸(择泰、ZOMETA)不得与钙或其他含二价阳离子的输注溶液(如乳酸林格液)混合,应作为单一静脉注射溶液与所有其他药物分开单独服用。
1)4毫克/100毫升单剂量即用型瓶
用于输注的唑来膦酸(择泰、ZOMETA)即用型溶液的瓶内装得过满,允许输注100毫升溶液(相当于4毫克唑来膦酸)。该溶液可直接用于患者,无需进一步制备。仅供一次性使用。
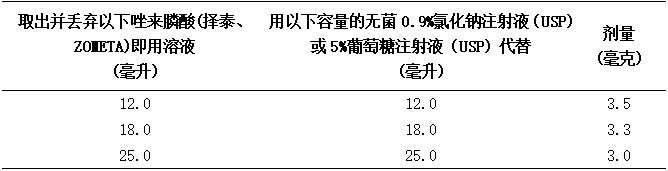
为基线CrCl小于或等于60毫升/分钟的患者制备减少剂量,从瓶中取出指定体积的唑来膦酸(择泰、ZOMETA)溶液,并更换为等体积的无菌0.9%氯化钠(USP)或5%葡萄糖注射液(USP)。向患者输注新制备的剂量调整溶液。遵循适当的无菌技术。正确丢弃先前取出的即用型溶液-不要储存或重复使用。
表:配制减少剂量的唑来膦酸(择泰、ZOMETA)即用瓶
如果在用输注介质稀释后未立即使用,为了保持微生物完整性,应将溶液在2°C至8°C下冷藏。然后,应在给药前将冷藏溶液平衡至室温。从稀释、在冰箱中储存到给药结束之间的总时间不得超过24小时。
2)4毫克/5毫升单剂量小瓶,用于静脉输注前稀释
用于静脉输注前稀释的唑来膦酸(择泰、ZOMETA)4毫克/5毫升小瓶中含有过量填充物,可抽出5毫升(相当于4毫克唑来膦酸)。应按照适当的无菌技术,立即将唑来膦酸(择泰、ZOMETA)(4毫克/5毫升)稀释在100毫升无菌0.9%氯化钠(USP)或5%葡萄糖注射液(USP)中,并通过静脉输注给予患者。请勿将未稀释的唑来膦酸(择泰、ZOMETA)(4毫克/5毫升)储存在注射器中,以避免意外注射。
要为基线CrCl小于或等于60毫升/分钟的患者制备减少的剂量,从药瓶中取出规定体积的唑来膦酸(择泰、ZOMETA)(4毫克/5毫升)用于所需剂量。
表:配制减量剂量唑来膦酸(择泰、ZOMETA)4毫克/5毫升单剂量稀释瓶

取出的唑来膦酸(择泰、ZOMETA) (4毫克/5毫升)溶液必须用100好的无菌0.9%氯化钠(USP)或5%葡萄糖注射液(USP)稀释。
如果在用输注介质稀释后未立即使用,为了保持微生物完整性,应将溶液在2°C至8°C下冷藏。然后,应在给药前将冷藏溶液平衡至室温。从稀释、在冰箱中储存到给药结束之间的总时间不得超过24小时。
4、给药方法
由于存在临床意义上的肾功能恶化风险,可能进展为肾衰竭,单剂量唑来膦酸(择泰、ZOMETA)不应超过4毫克,输注时间不应少于15分钟。在试验和上市后经验中,患者(包括接受经批准的4毫克剂量输注15分钟以上的患者)中发生了肾脏恶化、进展为肾衰竭和透析。在初始唑来膦酸(择泰、ZOMETA)剂量后,曾发生过这种情况。
1、恶性肿瘤高钙血症
2、肾毒性
3、急性期反应
4、矿物质和电解质异常
5、注射部位反应
6、眼部不良事件
7、多发性骨髓瘤与实体瘤骨转移
最常见的副作用为恶心、疲劳、贫血、骨痛、便秘、发热、呕吐和呼吸困难。
1、含有相同活性成分或属于同一药物类别的药物
唑来膦酸(择泰、ZOMETA)中的活性成分与Reclast(唑来膦酸)中的活性成分相同。接受唑来膦酸(择泰、ZOMETA)治疗的患者不应接受瑞卡斯特或其他双膦酸盐治疗。
2、水化和电解质监测
恶性肿瘤高钙血症患者必须在服用唑来膦酸(择泰、ZOMETA)之前充分补充水分。在患者充分复水前不应使用袢利尿剂,应谨慎与唑来膦酸(择泰、ZOMETA)联合使用,以避免低钙血症。唑来膦酸(择泰、ZOMETA)应与其他肾毒性药物一起谨慎使用。开始唑来膦酸(择泰、ZOMETA)治疗后,应仔细监测与标准高钙血症相关的代谢参数,如血清钙、磷和镁水平以及血清肌酸酐。如果出现低钙血症、低磷血症或低镁血症,可能需要短期补充治疗。
3、肾功能损害
唑来膦酸(择泰、ZOMETA)主要通过肾脏完整排出,而肾功能受损的患者发生不良反应的风险,特别是肾不良反应的风险可能更大。对于患有严重肾功能损害的患者,其安全性和药代动力学数据有限,且肾脏恶化的风险增加。先前存在的肾功能不全和多周期的唑来膦酸(择泰、ZOMETA)和其他双膦酸盐是随后发生唑来膦酸(择泰、ZOMETA)的肾脏恶化的危险因素。如果可能的话,应确定和管理易导致肾功能恶化的因素,如脱水或使用其他肾毒性药物。
只有在评估了治疗的风险和益处后,才应考虑对恶性肿瘤高钙血症伴严重肾功能损害患者进行唑来膦酸(择泰、ZOMETA)治疗。在临床研究中,排除了血清肌酸酐大于400mol/升或大于4.5毫克/分升的患者。
对于有严重肾功能损害的骨转移患者,不建议使用唑来膦酸(择泰、ZOMETA)治疗。在临床研究中,排除了血清肌酸酐大于265mol/升或大于3.0毫克/分升的患者,在564名接受唑来膦酸(择泰、ZOMETA)4毫克,15分钟输注治疗的患者中,只有8名基线肌酸酐大于2毫克/分升。肌酐清除率低于30毫升/分钟的患者存在有限的药代动力学数据。
4、颌骨骨坏死
据报告,颌骨坏死(ONJ)主要发生在接受静脉注射双膦酸盐(包括唑来膦酸(择泰、ZOMETA))治疗的癌症患者中。其中许多患者还在接受化疗和皮质类固醇治疗,这可能是ONJ病的危险因素。ONJ病的风险可能随着双膦酸盐暴露时间的延长而增加。
上市后经验和文献表明,基于肿瘤类型(晚期乳腺癌、多发性骨髓瘤)和牙齿状况(拔牙、牙周病、局部创伤,包括假牙安装不当)的ONJ报告频率较高。ONJ的许多报告涉及有局部感染体征(包括骨髓炎)的患者。
癌症患者应保持良好的口腔卫生,在接受双膦酸盐治疗前,应进行预防性牙科检查。
在治疗期间,如有可能,这些患者应避免进行侵入性牙科手术。对于在接受双膦酸盐治疗期间出现ONJ的患者,牙科手术可能会加重病情。对于需要进行牙科手术的患者,尚无数据表明停用双膦酸盐治疗是否可降低ONJ风险。治疗医师的临床判断应根据个人的获益/风险评估来指导每位患者的管理计划。
5、肌肉骨骼疼痛
根据上市后经验,在服用双膦酸盐[包括唑来膦酸(择泰、ZOMETA)]的患者中,曾有发生严重且偶尔会导致骨、关节和/或肌肉疼痛的报告。症状出现的时间从开始服用药物后的一天到几个月不等。如果出现严重症状,请停止使用。大多数患者停药后症状缓解。一个亚组在接受相同药物或另一种双膦酸盐的再激发时出现症状复发。
6、不典型的股骨转子下和骨干骨折
接受双膦酸盐治疗的患者(包括唑来膦酸(择泰、ZOMETA))中曾报告过非典型的转子下和股骨骨干骨折。这些骨折可发生在股骨干的任何位置,从小转子正下方到髁上扩口正上方,呈横向或短斜形,没有粉碎的证据。这些骨折发生在外伤很小或没有外伤之后。患者在出现完全性股骨骨折前数周至数月可能会出现大腿或腹股沟疼痛。骨折常为双侧;因此,在接受双膦酸盐治疗的股骨干骨折患者中,应对对侧股骨进行检查。也有这些骨折愈合不良的报告。许多病例报告指出,患者在骨折时也在接受糖皮质激素(如泼尼松或地塞米松)治疗。与双膦酸盐治疗的因果关系尚未确定。
任何有双膦酸盐暴露史的患者,如果在无外伤的情况下出现大腿或腹股沟疼痛,应怀疑为非典型骨折,并应进行评估。在对疑似患有非典型股骨骨折的患者进行评估之前,应根据个人受益风险评估,考虑停止唑来膦酸(择泰、ZOMETA)治疗。目前尚不清楚停止治疗后非典型股骨骨折的风险是否继续存在。
7、哮喘患者
虽然在唑来膦酸(择泰、ZOMETA)的临床试验中未观察到,但已有报告称接受双膦酸盐治疗的阿司匹林敏感性患者出现支气管收缩。
8、肝功能损害
使用唑来膦酸(择泰、ZOMETA)治疗肝功能不全患者的恶性肿瘤高钙血症的临床数据有限,这些数据不足以为这些患者的剂量选择或如何安全使用唑来膦酸(择泰、ZOMETA)提供指导。
9、低血钙症
使用唑来膦酸(择泰、ZOMETA)治疗的患者中曾报告过低钙血症。有报告称,严重低钙血症继发心律失常和神经系统不良事件(癫痫、手足抽搐和麻木)。在某些情况下,低钙血症可能危及生命。当唑来膦酸(择泰、ZOMETA)与已知会导致低钙血症的药物一起服用时,建议谨慎使用,因为可能会出现严重的低钙血症。开始服用唑来膦酸(择泰、ZOMETA)之前,应测量血清钙,并纠正低钙血症。为患者提供充足的钙和维生素d补充。
10、胚胎-胎儿毒性
根据动物研究的结果及其作用机制,对孕妇服用唑来膦酸(择泰、ZOMETA)可对胎儿造成伤害。在动物生殖研究中,根据曲线下面积(AUC),在母体暴露量大于或等于人类临床暴露量的2.4倍时,器官发生期间向妊娠动物给予唑来膦酸会导致胎儿畸形和胚胎-胎儿致死。双膦酸盐类药物[如唑来膦酸(择泰、ZOMETA)]可与骨基质结合,并在数周至数年内逐渐释放。如果女性在完成一个疗程的双膦酸盐治疗后怀孕,可能会有胎儿受损(如骨骼和其他异常)的风险。告知孕妇和有生殖潜力的女性对胎儿的潜在风险。告知有生殖潜力的女性在唑来膦酸(择泰、ZOMETA)治疗期间和之后使用有效避孕方法。
1、妊娠期
根据动物研究的结果及其作用机制,对孕妇服用唑来膦酸(择泰、ZOMETA)可对胎儿造成伤害。没有可用的孕妇数据来告知药物相关风险。在动物生殖研究中,基于AUC,在母体暴露量大于等于人类临床暴露量的2.4倍时,器官发生期间给予妊娠动物唑来膦酸(择泰、ZOMETA)导致胎儿畸形和胚胎-胎儿致死。双膦酸盐类药物[如唑来膦酸(择泰、ZOMETA)]可与骨基质结合,并在数周至数年内逐渐释放。如果女性在完成一个疗程的唑来膦酸(择泰、ZOMETA)治疗后怀孕,可能会有胎儿受损(如骨骼和其他异常)的风险。告知孕妇和有生殖潜力的女性对胎儿的潜在风险。
2、哺乳期
服用唑来膦酸(择泰、ZOMETA)后,尚不清楚zoledronic是否存在于人乳汁中,或是否会影响产奶量或母乳喂养的婴儿。唑来膦酸(择泰、ZOMETA)与骨长期结合,可能在数周至数年内释放。由于母乳喂养的儿童可能出现严重的不良反应,建议哺乳期妇女在唑来膦酸(择泰、ZOMETA)治疗期间和之后不要进行母乳喂养。
3、具有生殖潜力的男性和女性
开始使用唑来膦酸(择泰、ZOMETA)之前,验证具有生殖潜力的女性的妊娠状态。
对孕妇服用唑来膦酸(择泰、ZOMETA)可对胎儿造成伤害。zoledronic与骨长期结合,可能在数周至数年内释放。告知有生殖潜力的女性在唑来膦酸(择泰、ZOMETA)治疗期间和之后使用有效避孕方法。
根据动物研究,唑来膦酸(择泰、ZOMETA)可能会损害具有生殖潜力的女性的生育能力。
4、儿童用药
唑来膦酸(择泰、ZOMETA)不适合用于儿童。
5、老年用药
唑来膦酸(择泰、ZOMETA)在恶性肿瘤高钙血症中的临床研究包括34名65岁或以上的患者。与年轻患者相比,接受唑来膦酸(择泰、ZOMETA)治疗的老年患者的应答率或不良反应没有显著差异。唑来膦酸(择泰、ZOMETA)在治疗65岁以上多发性骨髓瘤和实体瘤骨转移患者中的对照临床研究显示,在老年和年轻患者中疗效和安全性相似。由于肾功能减退更常见于老年人,因此应特别注意监测肾功能。
对zoledronic或唑来膦酸(择泰、ZOMETA)的任何组分过敏者禁用。
已经报告了过敏反应,包括罕见的荨麻疹和血管性水肿病例,以及非常罕见的过敏反应/休克病例。
体外研究表明,唑来膦酸(择泰、ZOMETA)的血浆蛋白结合率较低,未结合部分在60%-77%之间。体外研究还表明,唑来膦酸(择泰、ZOMETA)不会抑制微粒体CYP450酶。体内研究表明,唑来膦酸(择泰、ZOMETA)不进行代谢,而是作为完整药物排泄到尿液中。
1、氨基糖苷类和降钙素
当双膦酸盐与氨基糖苷类或降钙素一起给药时,建议谨慎,因为这些药物可能对长期降低血清钙水平有叠加效应。这种效应在唑来膦酸(择泰、ZOMETA)临床试验中未见报道。
2、袢利尿剂
由于低钙血症的风险增加,当唑来膦酸(择泰、ZOMETA)与袢利尿剂联合使用时也应谨慎。
3、肾毒性药物
当唑来膦酸(择泰、ZOMETA)与其他潜在肾毒性药物一起使用时,应谨慎。
4、镇静剂
当与沙利度胺联合用药时,无需调整唑来膦酸(择泰、ZOMETA)4毫克的剂量。在一项针对24例多发性骨髓瘤患者的药代动力学研究中,唑来膦酸(择泰、ZOMETA)4 毫克作为15分钟输液单独给药或与沙利度胺联合给药(100毫克,第1-14天每日一次,200毫克,第15-28天每日一次)。
沙利度胺与唑来膦酸(择泰、ZOMETA)联合用药未显著改变唑来膦酸的药代动力学或肌酐清除率。
唑来膦酸(择泰、ZOMETA)急性过量用药的临床经验有限。在临床试验中,两名患者在5分钟内服用了唑来膦酸(择泰、ZOMETA)32毫克。两名患者均未出现任何临床或实验室毒性。过量用药可能导致临床上显著的低钙血症、低磷血症和低镁血症。临床相关的血清钙、磷和镁水平降低应分别通过静脉注射葡萄糖酸钙、磷酸钾或磷酸钠和硫酸镁来纠正。
在一项唑来膦酸(择泰、ZOMETA)4毫克治疗乳腺癌患者的开放标签研究中,一名女性患者错误地服用了48毫克单剂量的唑来膦酸(择泰、ZOMETA)。用药过量后两天,患者出现单次高热(38℃),治疗后消退。所有其他评估均正常,患者在用药过量七天后出院。
1例非霍奇金淋巴瘤患者接受唑来膦酸(择泰、ZOMETA)治疗,每日4毫克,连续4天,总剂量为16毫克。患者出现感觉异常和肝功能测试异常,GGT增加(近100单位/升,每个值未知)。该病例的结果尚不清楚。
在对照临床试验中,与15分钟静脉输注相同剂量相比,5分钟静脉输注唑来膦酸(择泰、ZOMETA)4毫克会增加肾毒性风险。在对照临床试验中,已显示与唑来膦酸(择泰、ZOMETA)4毫克相比,唑来膦酸(择泰、ZOMETA)8毫克与肾毒性风险增加相关,即使以15分钟静脉输注给药,且与恶性高钙血症患者的额外获益无关。
1、活性成分:zoledronic
2、非活性成分:甘露醇,USP,作为膨胀剂,注射水,柠檬酸钠,USP,作为缓冲剂。
注射剂
1、储存在25°C下;允许波动范围为15°C至30°C[参见USP控制的室温]。
2、丢弃未使用的部分。
诺华



互联网药品信息服务资格证书

孟加拉耀品国际授权书

孟加拉珠峰制药授权书

孟加拉伊思达制药授权书

孟加拉伊思达制药授权书

土耳其医院授权书
 正品保障
正品保障
 厂家直采
厂家直采
 专业药师
专业药师
 品类齐全
品类齐全