



2022年01月24日(丹麦瓦尔比) H. Lundbeck A/S (灵北制药) 宣布欧盟委员会已授予 Vyepti® (eptinezumab) 在欧盟 (EU) 的上市许可,用于预防性治疗患有偏头痛的成人(每月至少有4天偏头痛)。Vyepti是欧盟第1个也是唯一1个获批的用于预防偏头痛的静脉注射疗法。那么,Vyepti(艾普奈珠单抗)治疗发作性偏头痛的效果?
研究 1(NCT02559895) 纳入了有发作性偏头痛病史(每月头痛4-14天,其中至少4天为偏头痛天数)的成人。共有665例患者随机接受安慰剂 (N = 222)、100 mg VYEPTI(N = 221) 或300 mg VYEPTI(N = 222),每3个月一次,持续12个月。允许患者在试验期间同时使用急性偏头痛或头痛药物,包括偏头痛特异性药物(即曲坦类、麦角胺衍生物)。
该研究排除了有心血管疾病(高血压、缺血性心脏病)、神经系统疾病或脑血管疾病史的患者。
主要疗效终点是第1-3个月平均每月偏头痛天数较基线的变化。次要终点包括第1-3个月每月偏头痛天数较基线减少50%或以上、减少75%或以上的患者百分比。
患者的中位年龄为39岁(范围:18-71岁),84%为女性,84%为白人。基线时平均偏头痛发作频率约为每月8.6天,各治疗组相似。
与安慰剂相比,VYEPTI治疗显示主要疗效终点的统计学显著改善,如表2所示;次要终点也总结在表1中。
表1:研究1中的疗效终点结果
|
|
VYEPTI 100 mg
N = 221 |
VYEPTI 300 mg
N = 222 |
安慰剂
N = 222 |
|
每月偏头痛天数 (MMD)-第1-3个月 |
|
||
|
较基线变化 |
-3.9 |
-4.3 |
-3.2 |
|
与安慰剂的差异 |
-0.7 |
-1.1 |
|
|
p 值 |
0.018 |
<0.001 |
|
|
≥50%MMD应答者-第1-3个月 |
|
||
|
应答者% |
49.8% |
56.3% |
37.4% |
|
与安慰剂的差异 |
12.4% |
18.9% |
|
|
p 值 |
0.009* |
<0.001 |
|
|
≥75%MMD应答者-第1-3个月 |
|
||
|
应答者% |
22.2% |
29.7% |
16.2% |
|
与安慰剂的差异 |
6.0% |
13.5% |
|
|
p 值 |
NS** |
<0.001 |
|
图1:研究1中每月偏头痛天数较基线的变化
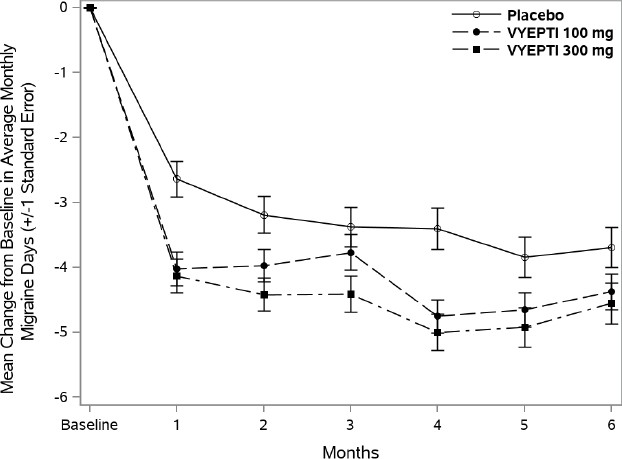
图2按治疗组以2天为增量显示了至第3个月平均每月偏头痛天数较基线的变化分布。
图2:研究1中按治疗组列出的第1-3个月平均每月偏头痛天数较基线变化的分布
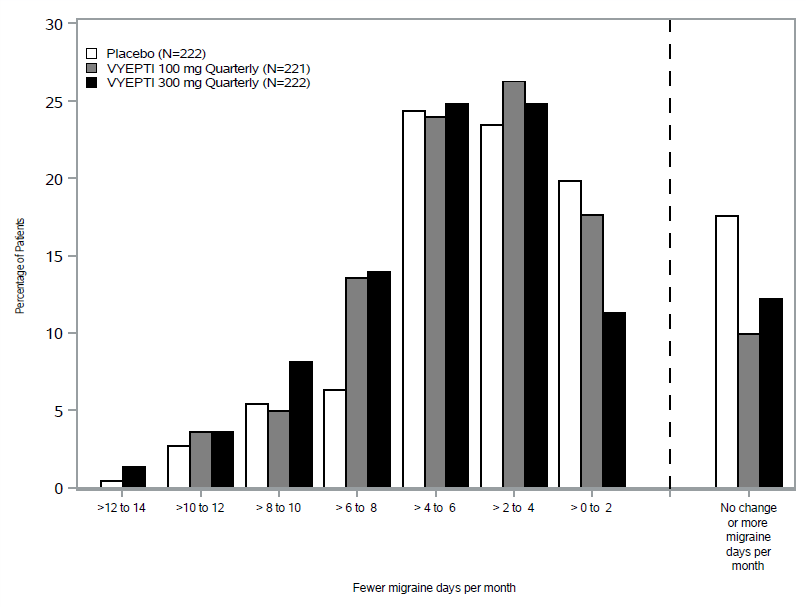
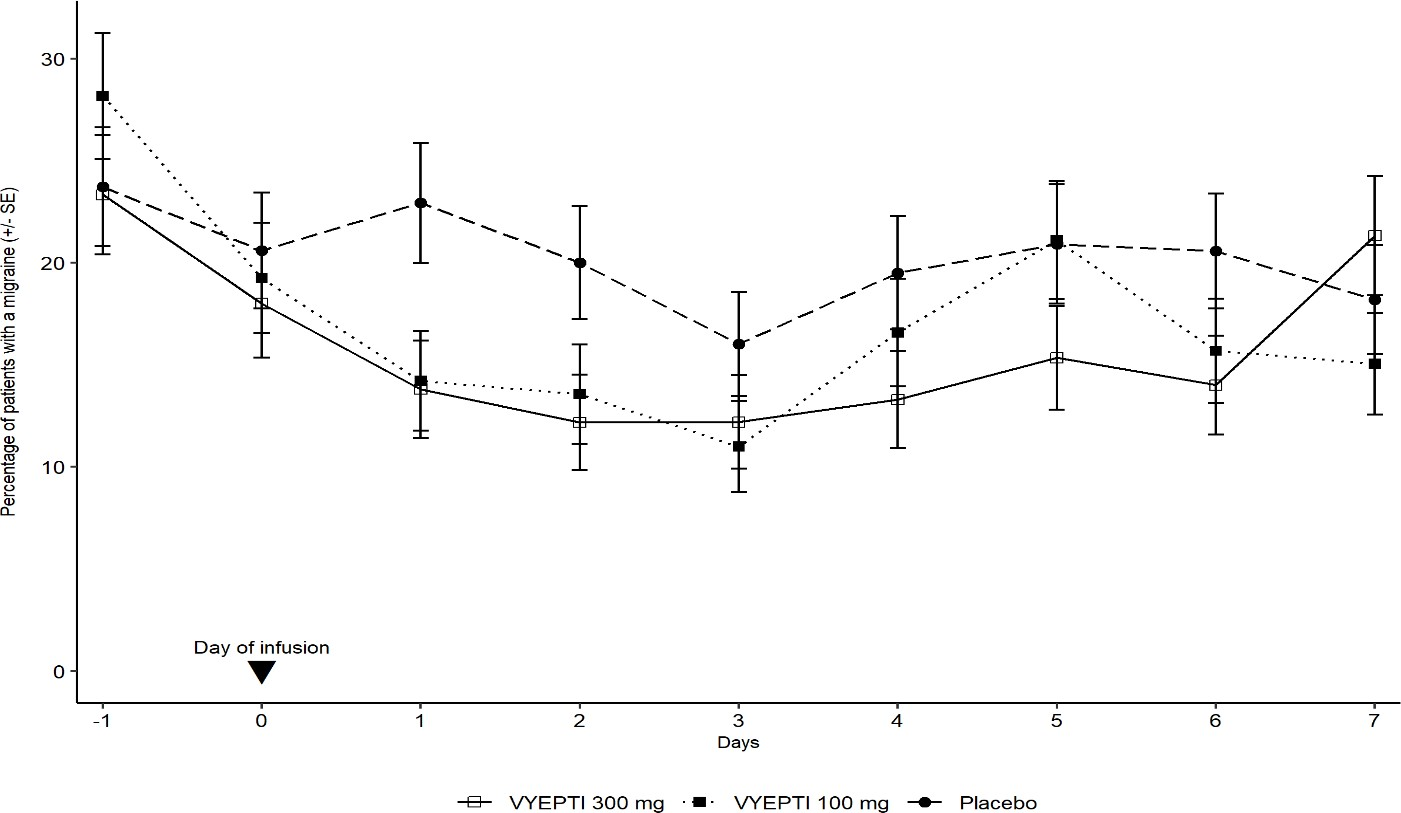
图3显示,在研究1中,与 VYEPTI 治疗患者相比,安慰剂治疗患者在治疗的前7天内的大多数天数发生偏头痛的百分比更高。
图3:研究1中从第-1天(输注前一天)至第7天发生偏头痛的患者百分比
相关热文推荐:Vyepti(艾普奈珠单抗)不良反应有哪些?
注:文章信息来源于网络,仅供医护人员内部讨论,不作为用药依据,具体用药指引,请咨询主治医师。
