免疫治疗作为近年来肿瘤治疗领域的新星,已经在多种类型的肿瘤中显示其疗效。头颈部鳞癌是一种具有高度免疫缺陷的肿瘤。大多数患者确诊时已是晚期,使用手术或放疗,5年生存率不足40%。
2019年,美国FDA批准帕博利珠单抗(Pembrolizumab,商品名:可瑞达,俗称“K药”)用于一线治疗转移性或不可手术切除的复发性头颈部鳞状细胞癌(HNSCC)。帕博利珠单抗是首个获批一线治疗转移性或不可切除的复发性头颈癌的PD-1疗法。
基于KEYNOTE-048研究(NCT02358031)结果:在CPS≥20的人群中,帕博利珠单抗单药组与EXTREME方案组相比,中位总生存期分别为14.9个月和10.7个月。在CPS≥1的人群中,帕博利珠单抗单药组与EXTREME方案组相比,中位总生存期分别为12.3个月和10.3个月。结果证明,帕博利珠单抗单用可以为头颈部鳞癌患者带来疗效确切、不良反应更小的治疗新选择。
医伴旅了解到目前正在开展帕博利珠单抗联合或不联合仑伐替尼治疗头颈部鳞状细胞癌的研究,符合临床项目报名标准的患者可以踊跃报名,我们将为大家提供最适合的临床项目。
试验药物:
帕博利珠单抗注射液
适应症:
头颈部鳞状细胞癌
临床试验信息:
试验分类:安全性和有效性 试验目的:评估帕博利珠单抗联合仑伐替尼对比帕博利珠单抗联合安慰剂在PD-L1选择的复发性或转移性头颈部鳞状细胞癌一线治疗的有效性和安全性 试验分期:III期 设计类型:平行分组 随机化:随机化 盲法:双盲 试验范围:国际多中心试验 年龄:18岁(最小年龄)至 无上限 (最大年龄) 性别:男+女 健康受试者:无
主要入选标准:
1.具有局部治疗无法治愈的经组织学确诊的R/M HNSCC。 2.原发肿瘤位于口咽、口腔、下咽或喉。 3.在签署知情同意时年龄为18岁及以上的男性或女性。 4.存在通过BICR根据RECIST 1.1评估的可测量疾病。 5.存在通过中心实验室测定的PD-L1阳性(CPS≥1)肿瘤。 6.患有口咽癌的受试者必须有HPV状态检测结果。
主要排除标准:
1.在随机分组前6个月内有任何活动性肿瘤出血的症状或体征的证据。 2.有大血管侵犯/浸润的放射影像学证据或肿瘤>90度邻接或包绕大血管。 3.有头颈部疾病的再放射史,包括头颈部癌的颈部、锁骨下或锁骨上淋巴结。 4.皮肤表面有溃疡和/或真菌形成。 5.有任何禁忌症史或对帕博利珠单抗或仑伐替尼的任何成分有严重超敏反应(≥3级)。 6.既往存在≥3级的胃肠道或非胃肠道瘘管。
主要研究中心所在地(具体启动情况以后期咨询为准):
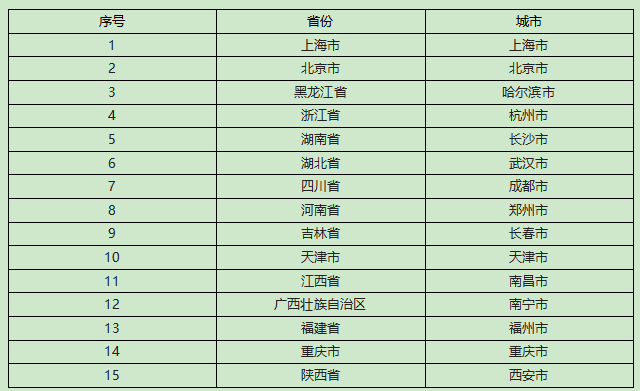
联系方式:
如果您身边有合适的患者欢迎与我们联系。24小时服务热线:400-001-2811

参与临床试验,不仅可以使用最新的治疗方法,医生还会密切关注您的病情状况。病情严重的患者,现行疗法效果不佳或者无力承担费用,参加临床试验免费尝试新的治疗方法,不管是对患者本人还是家属都是一种不错的选择。欢迎大家踊跃报名。注:最终能否入选需要由研究医生判定。
注:文章信息来源于网络,仅供医护人员内部讨论,不作为用药依据,具体用药指引,请咨询主治医师。