



美国已经批准了达雷木单抗(Darzalex ,daratumumab)注射剂,联合硼替佐米(Velcade)、环磷酰胺(cyclophosphamide)和地塞米松(dexamethasone)治疗诊断的轻链型(AL)淀粉样变疾病,这是第一种也是唯一一种治疗该疾病的方法。
轻链型(AL)淀粉样变疾病,每年在美国影响约4500人。当骨髓中的血浆细胞产生淀粉样蛋白沉积物时,就会发生这种病,这种沉积物可能会在重要器官(尤其是心脏、肾脏和肝脏)中积聚,最终导致器官恶化。诊断往往被延误,约30%的患者在诊断后的第一年内死亡。
美国食品和药物管理局基于3期ANDROMEDA研究的血液学完全缓解率数据,授予达雷木单抗用于AL淀粉样变的加速批准。
在2020年6月召开的欧洲血液学协会第25届年会(EHA)上公布了3期ANDROMEDA研究的积极结果。
结果显示,与单独使用VCd相比,在硼替佐米、环磷酰胺和地塞米松(VCd)的联合用药中加入达雷木单抗可大幅改善血液学缓解,并延迟器官衰竭的时间。
ANDROMEDA是一项正在进行的随机、开放标签研究,涉及388名初治患者,他们患有可测量的血液学疾病,其中一个或多个器官受到影响。
约三分之一(37%)的患者因轻链型(AL)淀粉样变导致严重的心脏功能障碍(心脏III期);40%为心脏II期;23%为I期。
患者被随机分配到接受达雷木单抗注射加VCd联合治疗或单用VCd。
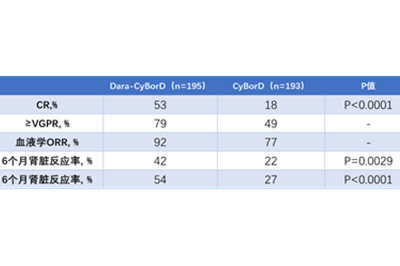
主要终点是总体血液学完全缓解。在11.4个月的中位随访中,达雷木单抗组有53%的患者经历了完全缓解,而VCd组为18%。
图片来源于news.medlive.cn,侵删
在次要终点主要器官恶化无进展生存期方面,达雷木单抗组占优势。其他次要终点方面也是达雷木单抗组表现强势,包括6个月时的心脏反应率和肾脏反应率。
各组死亡人数相似(daratumumab,27;VCd,29)。
安全性情况与之前在daratumumab或VCd单药中观察到的一致。超过5%的患者发生了常见3到4级治疗相关突发不良事件,包括淋巴细胞减少、肺炎、腹泻、充血性心力衰竭、中性粒细胞减少、晕厥和外周水肿。
达雷木单抗不适用,也不推荐用于治疗对照临床试验以外的有NYHA IIIB级或IV级心脏病或Mayo IIIB期疾病的AL淀粉样变患者。
参考资料:FDA Approves First and Only Treatment for AL Amyloidosis
注:文章信息来源于网络,仅供医护人员内部讨论,不作为用药依据,具体用药指引,请咨询主治医师。
