酮洛芬巴布贴为非甾体抗炎药(NSAIDs)类经皮吸收制剂,主要通过抑制前列腺素的合成,发挥局部镇痛和抗炎作用。其设计为亲水性巴布剂(水凝胶贴剂),通过皮肤渗透将活性成分递送至病灶局部,减轻炎症反应和疼痛。由于经皮给药避免了肝脏首过效应,并维持了局部较高的血药浓度,适用于治疗浅表性软组织和关节的慢性疼痛与急性炎症。然而,临床使用时需重点关注其潜在的皮肤光敏反应和接触性皮炎风险。
药品称呼
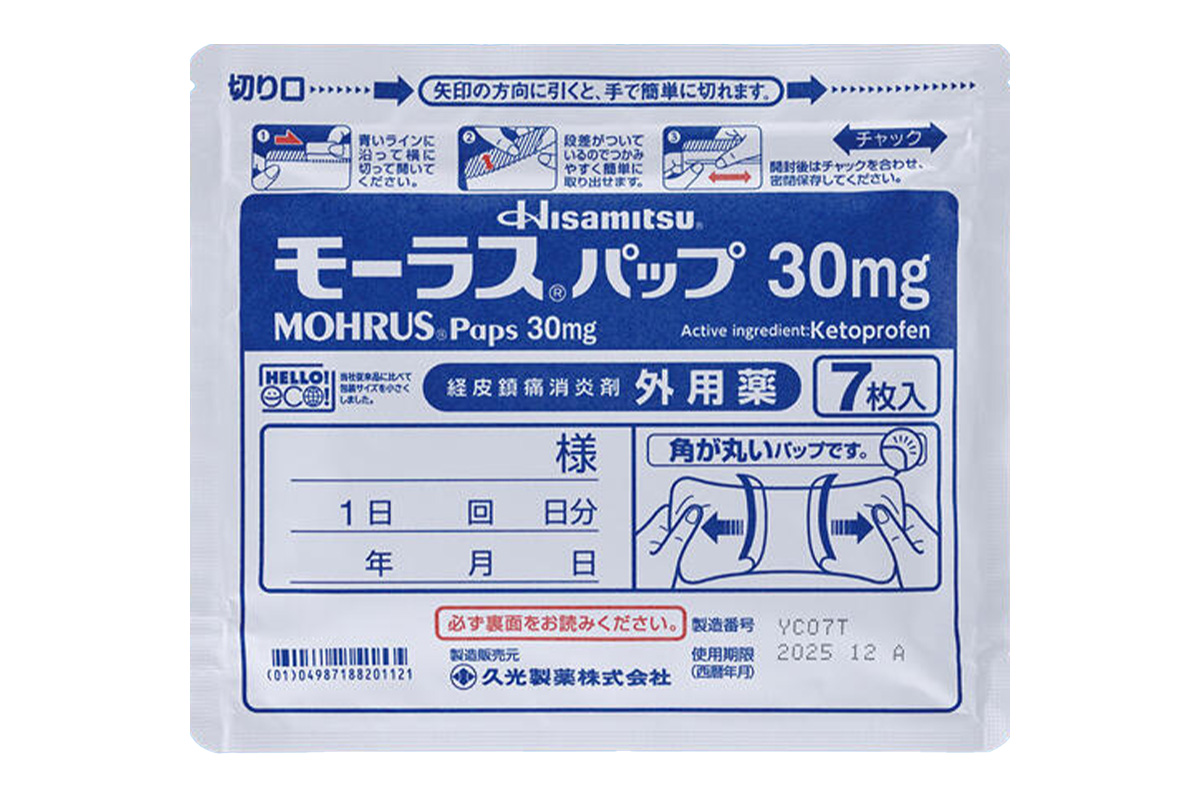
通用名称:酮洛芬巴布贴、Ketoprofen
商品名称:Mohrus
适应靶点
酮洛芬巴布贴为非选择性环氧合酶(COX)抑制剂,主要作用于花生四烯酸代谢通路,抑制前列腺素(PG)的合成,从而阻断炎症介质的产生,达到消炎镇痛的效果。
适应症和适应人群
酮洛芬巴布贴适用于以下疾病及症状的镇痛、消炎:骨关节炎(变形性关节症)、肩关节周围炎(肩周炎)、腱鞘炎、肌腱炎及腱周炎、肱骨外上髁炎(网球肘等)、肌肉痛、外伤后的肿胀及疼痛(如扭伤、挫伤)。
规格与性状
规格:30mg*7枚/袋。
性状:酮洛芬巴布贴为白色至淡黄白色的膏体,涂布于支持体上,表面覆盖有防粘衬膜(剥离膜)。制剂尺寸为10cm×14cm,具有特异的芳香气味。识别代码为HP315P。
主要成分
有效成分:每贴含有日本药局方酮洛芬(Ketoprofen)30mg。
添加剂:l-薄荷醇、羟苯甲酮(氧苯酮/Oxybenzone)、克罗米通、合成硅酸铝、香料、二氧化钛、明胶、浓甘油、聚丙烯酸部分中和物、聚乙烯醇(部分皂化物)及其他3种成分。
用法用量
标准剂量:每日2次,将酮洛芬巴布贴贴敷于患部。
使用注意事项:
请勿用于损伤皮肤、粘膜、湿疹或皮疹部位,以免引起皮肤刺激。
酮洛芬巴布贴为对症治疗药物,而非对因治疗。
用于慢性疾病(如骨关节炎)时,应考虑药物疗法以外的其他治疗方案。
具体您可以阅读酮洛芬巴布贴完整用法用量信息,建议在医生的指导下正确用药。推荐文章:酮洛芬巴布贴的用法用量。
不良反应
重大副作用
休克、过敏反应(发生率不明,<0.1%):可能出现荨麻疹、呼吸困难、面部水肿等症状。
哮喘发作诱发(阿司匹林哮喘,<0.1%):表现为干性啰音、喘鸣、呼吸困难感。通常在贴敷后数小时内发生。
接触性皮炎(<5%,严重病例发生率不明):贴敷部位可能出现皮疹、发红、瘙痒、刺激感、红斑,严重时可发展为肿胀、水疱、糜烂、色素沉着或色素脱失,甚至全身扩散。部分病例在使用数日后才出现。
光敏反应(发生率不明):贴敷部位暴露于紫外线后,可能引发严重瘙痒、红斑、皮疹、刺激感、肿胀、水疱或糜烂,甚至全身化。症状可能在停药后数日至数月内出现。
其他副作用
皮肤局部(0.1%~<5%):皮疹、发红、肿胀、瘙痒、刺激感、水疱/糜烂、色素沉着。
皮肤局部(<0.1%):皮下出血。
过敏反应(发生率不明):荨麻疹、眼睑水肿、面部水肿。
具体您可以阅读酮洛芬巴布贴副作用信息,建议在医生的指导下正确用药。推荐文章:酮洛芬巴布贴的副作用。
注意事项
重要的基本注意事项
接触性皮炎与光敏反应管理:
无论是否接触紫外线,均可能发生接触性皮炎。若出现皮疹、发红、瘙痒、刺激感等,应立即停药,遮光保护患部并就医。
为防止光敏反应,用药期间及停药后一段时间内,无论天气如何,均应避免户外活动。日常外出时,需用衣物、护具等遮盖贴敷部位。应穿着不易透过紫外线的深色衣物(白色或薄料衣物可能透过紫外线)。
由于症状可能在用药后数日或停药后数月至出现,患者需长期保持警惕。
治疗性质:需明确酮洛芬巴布贴为对症治疗药物,不能替代针对病因的治疗。
慢性病管理:用于慢性病(如骨关节炎)时,应考虑综合治疗方案,不应仅依赖药物。
特殊人群用药
【孕妇】妊娠晚期禁用。使用酮洛芬外用制剂可能导致胎儿动脉导管提前收缩。妊娠期(除晚期外)仅在治疗获益大于风险时使用。应限制在最小必要剂量和最短时间内。有报道显示,妊娠中期使用酮洛芬可能导致羊水过少;COX抑制剂(口服或栓剂)可能导致胎儿肾功能障碍、尿量减少及羊水过少。
【哺乳期女性】说明书中尚未明确。
【具有生殖潜力的男性和女性】说明书中尚未明确。
【儿童使用】尚未在儿童人群中进行过临床试验,因此不推荐儿童使用。
【老年人使用】需谨慎使用,密切观察贴敷部位的皮肤状态。上市后调查数据显示,65岁以上老年患者接触性皮炎发生率显著高于65岁以下患者。
【肾功能损害】说明书中尚未明确。
【肝功能损害】说明书中尚未明确。
禁忌症
以下患者禁止使用酮洛芬巴布贴:
对酮洛芬巴布贴任何成分有过敏史者。
阿司匹林哮喘(NSAIDs诱发哮喘发作)或有该病史者。
对噻洛芬酸、舒洛芬、非诺贝特,以及含有羟苯甲酮(氧苯酮)和奥克立林的产品(如防晒霜、香水)有过敏史者(存在交叉过敏风险)。
有光敏反应既往史者。
妊娠晚期的女性。
药物相互作用
说明书中尚未明确。
药物过量
说明书中尚未明确。
药代动力学
吸收
单次给药:健康成年男性背部贴敷1枚(12小时),吸收率约为给药量的13.3%。动物实验显示,在去除角质层的损伤皮肤上,吸收率可达97.4%,提示皮肤屏障受损时全身暴露量显著增加。
血清浓度:单次贴敷12小时后,血清浓度达到43.11ng/mL,48小时后基本从血清中清除。
分布
局部穿透:在骨关节炎患者中,给药部位下方的皮肤、皮下脂肪、肌肉及滑膜中的药物浓度均高于血清浓度,呈浓度梯度递减(浅层组织浓度高于深层组织)。
组织分布:动物实验表明,正常皮肤给药后,药物在4小时达到血药峰浓度,6小时达到筋膜及肌肉峰浓度;在损伤皮肤上,所有组织在2小时内即达峰浓度。
代谢与排泄
排泄途径:主要以代谢产物形式经肾脏排泄。
单次给药:给药后48小时内完成大部分排泄,尿中排泄量约占吸收量的35.8%。
反复给药:每日2次连续给药,尿中排泄量在7天后趋于稳定,停药后迅速减少。
贮存方法
室温保存。有效期3年。
研发公司
日本久光制药