




12岁以上未满70岁(未满18岁仅限体重40kg以上)的以SARS-CoV-2引起的传染病患者为对象,第一天服用本品375mg,第2天至第5天,每日1次口服本品125mg时,以研究本剂的有效性及安全性为目的,对安慰剂我们进行了随机双盲平行组间比较试验。
主要评价项目是由SARS-CoV-2引起的传染病的5个症状恢复的时间(※1 )认为。
(※1 ) 由SARS-CoV-2引起的感染症的5个症状〔①倦怠感或疲劳感、②发热、③鼻涕或鼻塞、④喉咙痛、⑤咳嗽〕的各症状由被试验者本人分为4个阶段:
(0:无,1 :轻度、2 :中度、3 :重度)评估,痊愈定义为5症所有症状都持续以下状态至少24小时的情况被认为是。
对于SARS-Cov一2感染发病前就存在的症状,且受试者在基线(服药前检查)时判断为恶化的,基线时症状的严重程度应改善或保持中度或轻度﹐中度或轻度基线时轻度或轻度应改善或保持轻度或重度。严重程度的状态应改善或维持在轻度以下。
对于在SARS-Cov-2感染发病前就存在的、受试者判断在基线(服药前检查)时没有恶化的原有症状,在基线时严重的低于严重,在基线时中等的低于中等,在基线时严重的低于严重。轻度到低于轻度,病情的严重程度保持或改善。
上述以外的症状[SARS-CoV-2感染前存在不存在,在基线(给药前检查)点以后开始出现的症状是指没有的状态。
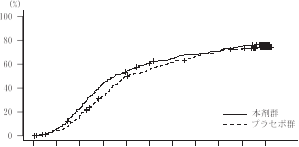
在被随机化的1215例(日本人662例)中,基线的鼻咽拭子标本经定性RT-PCR判断为阳性,而且从发现COVID-19症状到随机分配的时间为72点不足690例中,主要评价项目的结果如下表。
| 本剂组 | 安慰剂组 |
例数* | 336 | 321 |
复原计数 | 254 | 233 |
由SARS-cov-2弓|起的 SARS-CoV-2感染。 5症状恹复的中位时间(小时) | 167.9 | 192.2 |
p值** | 0.0407 | - |
风险比[95%置信区间]+ | 1.14[0.95,1.36] | - |
**显著性水平双方都是5%,有无接种SARS-Cov-2感染的疫苗Peto-Prentice的分层泛化Wilcoxo测试,没有任何东西作为分层。
+按层划分对SARS-CoV-2引起的传染病有无接种疫苗Cox危险模型。
免责声明: 以上内容整理于FDA说明书、DRUGS及网络,仅作信息交流之目的,文中观点不代表医伴旅立场,亦不代表医伴旅支持或反对文中观点。本文也不是治疗方案推荐。页面内容仅供医学药学专业人士阅读参考,具体用药请咨询主治医师,本站只做信息展示,不销售药品。如需获得治疗方案指导,请前往正规医院就诊。
参考资料: 日本药监局,更新于2024年12月的说明书https://www.info.pmda.go.jp/go/pack/6250052F1023_2_09/?view=frame&style=XML&lang=ja