



研究1
研究1是一项在 RRMS 患者中开展的2年、随机、开放标签、评定者设盲、活性对照药物(干扰素β-1a 44 μg,皮下注射,每周3次)对照研究。进入研究1的患者扩展残疾状态量表 (EDSS) 评分为5分或以下,在接受干扰素β或醋酸格拉替雷治疗期间必须经历至少一次复发。
患者随机接受LEMTRADA(n = 426) 或干扰素β-1a(n = 202) 治疗。基线时,平均年龄为35岁,平均病程为4.5年,平均 EDSS 评分为2.7。
临床结局指标为2年内的年化复发率 (ARR) 和至确认残疾进展的时间。确认的残疾进展定义为较基线 EDSS 增加至少1分(基线 EDSS 为0的患者增加1.5分)持续6个月。MRI结局指标为 T2 病灶体积的变化。
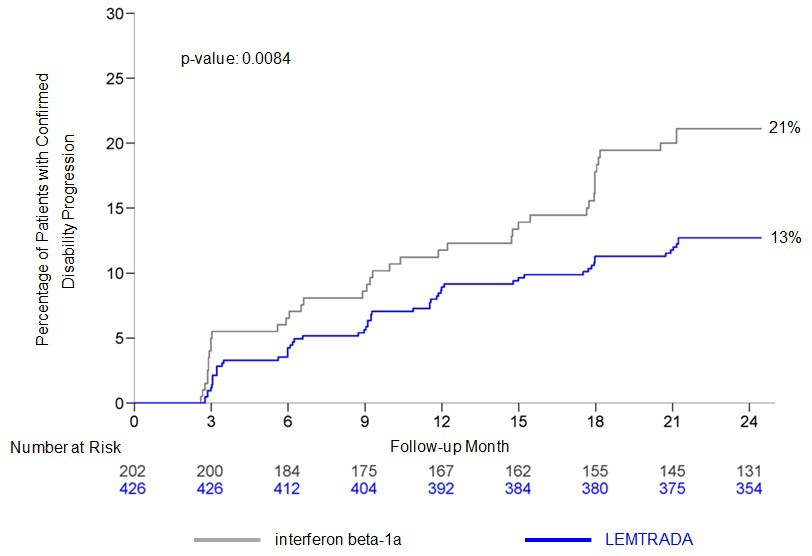
LEMTRADA 治疗患者的年化复发率显著低于干扰素β-1a治疗患者。与干扰素β-1a相比,LEMTRADA治疗至6个月证实的残疾进展发生的时间显著延迟。治疗组之间 T2 病灶体积的变化无显著差异。研究1的结果见表2和图1。
表2:研究1的临床和 MRI 结果
| LEMTRADA (N = 426) | 干扰素β-1a 44 μg(N = 202) | p 值 |
临床结局 | |||
年化复发率 | 0.26 | 0.52 | <0.0001 |
相对减少 | 49% |
|
|
第2年残疾进展的患者比例 | 13% | 21% | 0.0084 |
相对风险降低 | 42% |
|
|
第2年保持无复发的患者百分比 | 65% | 47% | <0.0001 |
MRI 结局 | |||
T2 病灶体积较基线的百分比变化 | -1.3 | -1.2 | 0.14 |
图1:至6个月确认残疾进展的时间(研究1)
研究2
研究2是一项在 RRMS 患者中开展的2年、随机、开放标签、评定者设盲、活性对照药物(干扰素β-1a 44 μg,皮下注射,每周3次)对照研究。进入研究2的患者 EDSS 评分≤3,既往未接受过多发性硬化症治疗。
患者随机接受LEMTRADA(n = 376) 或干扰素β-1a(n = 187) 治疗。基线时,平均年龄为33岁,平均病程为2年,平均 EDSS 评分为2。
临床结局指标为2年内的年化复发率 (ARR) 和至证实残疾进展的时间,如研究1中所定义。MRI结局指标为 T2 病灶体积的变化。
LEMTRADA 治疗患者的年化复发率显著低于干扰素β-1a治疗患者。在至证实残疾进展的时间和主要 MRI 终点(T2病变体积的变化)方面,治疗组间无显著差异。研究2的结果见表3。
表3:研究2的临床和 MRI 结果
| LEMTRADA (N = 376) | 干扰素β-1a 44 μg(N = 187) | p 值 |
临床结局 | |||
年化复发率 | 0.18 | 0.39 | <0.0001 |
相对减少 | 55% |
|
|
第2年残疾进展的患者比例 | 8% | 11% | 0.22 |
相对风险降低 | 30% |
|
|
第2年保持无复发的患者百分比 | 78% | 59% | <0.0001 |
MRI 结局 | |||
T2 病灶体积较基线的百分比变化 | -9.3 | -6.5 | 0.31 |



互联网药品信息服务资格证书

孟加拉耀品国际授权书

孟加拉珠峰制药授权书

孟加拉伊思达制药授权书

孟加拉伊思达制药授权书

土耳其医院授权书
 正品保障
正品保障
 厂家直采
厂家直采
 专业药师
专业药师
 品类齐全
品类齐全