




Kaftrio、Trikafta、依伐卡托/替扎卡托/依来沙卡托复合制剂、Elexacaftor/Tezacaftor/Ivacaftor
年龄在2岁及以上的囊性纤维化(CF)患者。[ 详情 ]
温馨提示: 图片来自公开渠道(如FDA官网、Drugs官网、原研药厂官网等),仅供参考。
在两项双盲对照试验中评估了kaftrio对12岁及以上囊性纤维化患者的疗效:
1、试验准备
(1)试验1是一项为期24周的随机、双盲、安慰剂对照研究,研究对象为一个等位基因上有F508del突变,而另一个等位基因上没有突变的患者,该突变导致无CFTR蛋白或CFTR蛋白对ivacaftor和tezacaftor/ivacaftor无反应。本试验需要至少140名患者完成4周计划,和至少100名患者完成12周计划。
(2)试验2是在F508del突变纯合子患者中进行的的随机、双盲、活性对照研究,为期4周。
2、试验结果
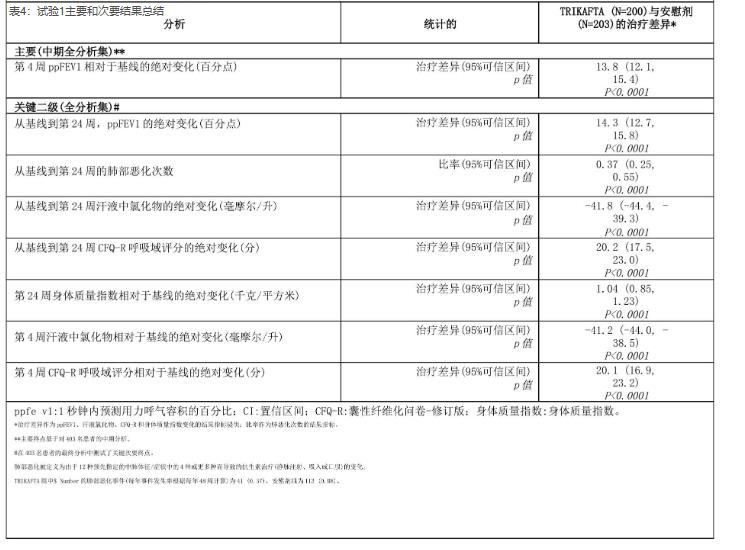
(1)试验1评估了403名年龄在12岁及以上(平均年龄26.2岁)的囊性纤维化患者的用药情况。基线ppFEV1为61.4%。中期分析时评估的主要终点是第4周时ppFEV1相对于基线ppFEV1的平均绝对变化。
在接受试验的403名患者中,第4周的ppFEV1相对于基线的平均绝对出现变化,kaftrio和安慰剂之间的治疗差异为13.8%,从基线到第24周,kaftrio和安慰剂之间的ppFEV1平均绝对变化的治疗差异为14.3%。综合来看,无论年龄、基线ppFEV1、性别和地理区域如何,均观察到ppFEV1的改善,试验1中主要和次要结果的总结见表4。
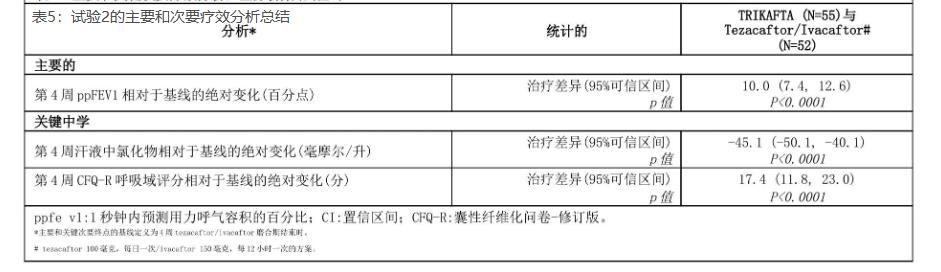
(2)试验2评估了107名12岁及以上(平均年龄28.4岁)的囊性纤维化患者的用药情况,在使用tezacaftor/ivacator进行为期4周的开放性磨合期后,基线平均ppFEV1为60.9%。主要评估终点是双盲治疗期第4周ppFEV1相对于基线ppFEV1的平均绝对变化。次要疗效终点是第4周时汗液氯化物和CFQ-R呼吸域评分相对于基线的绝对变化。
与使用tezacaftor/ivacaftor相比,使用kaftrio治疗的患者的ppFEV1改善10.0%,具有统计学显著性。在试验第15天时第一次评估中观察到ppFEV1平均改善。无论龄、性别、基线ppFEV1和地理区域如何,均观察到患者用药后ppFEV1的改善,主要和次要结果汇总见表5。
参考资料: FDA说明书更新于2025年9月25日,说明书网址:https://www.accessdata.fda.gov/scripts/cder/daf/index.cfm?event=overview.process&ApplNo=212273


