伐度司他是一种缺氧诱导因子脯氨酰羟化酶(HIF-PH)抑制剂,用于治疗慢性肾脏病(CKD)引起的贫血。该药通过模拟缺氧状态,促进内源性促红细胞生成素(EPO)的生成,刺激红细胞生成。适用于接受透析至少3个月的成年CKD患者。
药品称呼
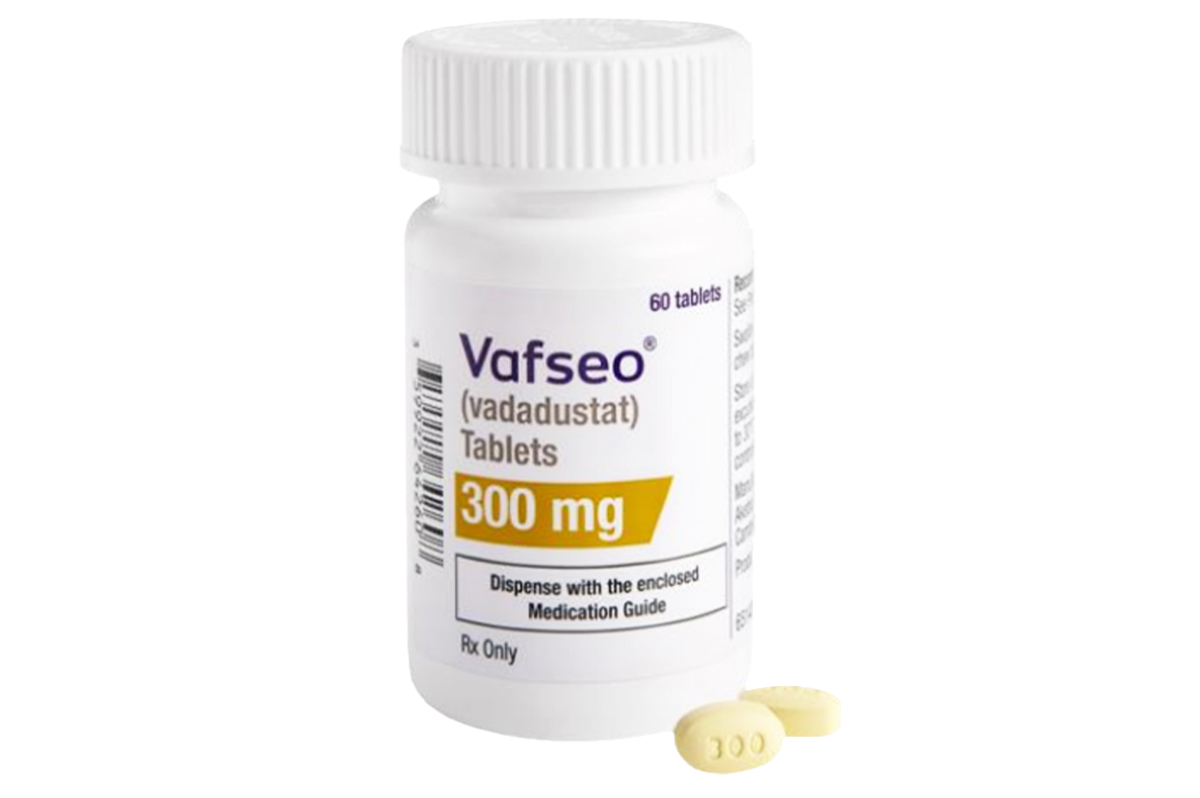
通用名称:伐度司他、Vadadustat
商品名称:Vafseo
适应靶点
HIF脯氨酰羟化酶(HIF-PH)1、2、3亚型。
适应症和适应人群
适应症:用于治疗慢性肾脏病(CKD)引起的贫血。
适应人群:接受透析至少3个月的成年患者。
限制使用:未显示改善患者的生活质量、缓解疲劳或提升健康状况。不用于需立即纠正贫血的输血替代治疗。不用于非透析CKD患者的贫血治疗。
规格与性状
规格:300mg*60片/瓶;
性状:300mg为椭圆形、黄色,刻有“VDT”和“300”。
主要成分
活性成分:伐度司他。
辅料:胶体二氧化硅、羟丙甲纤维素、硬脂酸镁、微晶纤维素、淀粉羟乙酸钠。
包衣成分:聚乙烯醇、聚乙二醇(PEG)、滑石粉。
着色剂:300mg:二氧化钛、黄色氧化铁。
用法用量
1.治疗前与治疗中评估
评估贫血原因及铁储备情况,排除其他贫血原因(如维生素缺乏、出血等)。
若血清铁蛋白<100mcg/L或转铁蛋白饱和度<20%,应补充铁剂。
治疗前及治疗期间需监测血红蛋白(Hb)、ALT、AST、总胆红素。
2.重要给药信息
个体化给药,使用最低有效剂量以减少输血需求。
Hb目标值不应超过11g/dL。
整片吞服,不可掰开、碾碎或咀嚼。
可与或不与食物同服。
漏服时应尽快补服,若已接近下一次服药时间则跳过,不可双倍补服。
3.推荐起始剂量
未使用ESA的患者:300mg,每日一次
由ESA转换而来:300mg,每日一次
转换期间若Hb<9g/dL,可考虑输血或ESA救援治疗。
若使用救援性ESA,需根据其类型暂停伐度司他:
依泊汀:最后一次给药后2天
达依泊汀α:最后一次给药后7天
甲氧基聚乙二醇-epoetinβ:最后一次给药后14天
4.治疗反应监测与剂量调整
起始或调整剂量后每2周监测Hb,稳定后每月一次。
剂量调整频率不超过每4周一次,下调可更频繁。
剂量以150mg为增量调整,范围150–600mg。
若Hb上升过快(>1g/dL/2周或>2g/dL/4周),应中断或减量。
若Hb>11g/dL,应中断给药直至Hb≤11g/dL,恢复时剂量减少150mg。
若治疗24周后Hb无临床意义上升,应停止治疗并评估其他原因。
5.药物相互作用导致的剂量调整
应在口服铁剂、含铁产品或含铁磷酸盐结合剂前至少1小时服用。
应在非含铁磷酸盐结合剂前1小时或后2小时服用。
具体您可以阅读伐度司他完整用法用量信息,建议在医生的指导下正确用药。推荐文章:伐度司他的用法用量。
不良反应
最常见不良反应(≥10%):高血压、腹泻。
严重不良反应:血栓事件(心梗、卒中、静脉血栓、血管通路血栓)、肝毒性、高血压加重或高血压危象、癫痫、胃肠道糜烂或出血、恶性肿瘤风险。
其他常见不良反应(≥5%):头痛、恶心、疲劳、腹痛、呕吐、头晕、呼吸困难、动静脉瘘血栓、透析相关并发症。
具体您可以阅读伐度司他完整副作用信息,建议在医生的指导下正确用药。推荐文章:伐度司他的副作用。
注意事项
1.血栓风险增加
可导致致命性动脉/静脉血栓事件。避免近期(3个月内)有心梗、卒中或急性冠脉综合征病史的患者使用。使用最低有效剂量,避免Hb>11g/dL。
2.肝毒性
可能导致肝细胞损伤。治疗前及治疗前6个月每月监测ALT、AST、胆红素,之后按临床需要监测。若ALT/AST>3×ULN或伴胆红素>2×ULN,应停药。
3.高血压
禁忌用于未控制的高血压患者。治疗期间监测血压,调整降压治疗方案。
4.癫痫
监测新发癫痫、前兆症状或发作频率变化。
5.胃肠道糜烂
尤其高风险人群:有胃肠道溃疡史、使用相关药物、吸烟、饮酒者。
6.非透析CKD患者
安全性未确立,不推荐使用。
7.恶性肿瘤
不推荐用于活动性恶性肿瘤患者。
特殊人群用药
【孕妇】数据不足,存在胎儿风险。仅在获益大于潜在风险时使用。
【哺乳期女性】药物可能进入乳汁,建议治疗期间及末次剂量后2天内停止哺乳。
【具有生殖潜力的男性和女性】说明书中尚未明确。
【儿童使用】安全性和有效性未确立。
【老年人使用】与年轻患者相比,安全性和有效性无显著差异。
【肾功能损害】仅适用于透析患者。非透析患者禁用。
【肝功能损害】不建议用于肝硬化或活动性急性肝病患者。
禁忌症
对伐度司他或任何成分过敏者;未控制的高血压患者。
药物相互作用
1.其他药物对伐度司他的影响
铁剂与磷酸盐结合剂:降低伐度司他暴露量,应错开服用。
OAT1/OAT3抑制剂(如丙磺舒、利福平):可能增加伐度司他AUC,需监测Hb反应及不良反应。
2.伐度司他对其他药物的影响
BCRP底物(如柳氮磺吡啶):可能增加其暴露量,需监测不良反应。
他汀类药物:
辛伐他汀:起始剂量不超过5mg/日,最大20mg/日
瑞舒伐他汀:最大剂量不超过5mg/日
OAT3底物(如呋塞米、西格列汀):可能增加暴露量,需监测不良反应。
药物过量
可能导致Hb过度升高。
处理方式:减量或停药,必要时透析(约16%药物可被透析清除)。无特异性解毒剂。
药代动力学
吸收:Tmax约2–3小时,食物无显著影响。
分布:蛋白结合率≥99.5%,不分布于红细胞。
代谢:主要通过UGT酶葡萄糖醛酸化。
排泄:主要经尿液(58.9%)和粪便(26.9%)排出。
半衰期:约9.2小时(透析患者)。
特殊人群:年龄、性别、种族、中度肝损无显著影响;重度肝损数据不足。
贮存方法
贮存于20°C–25°C(68°F–77°F),允许在15°C–30°C之间短时存放。避光防潮,置于儿童不可接触处。
研发公司
美国Akebia(美国艾可比亚)