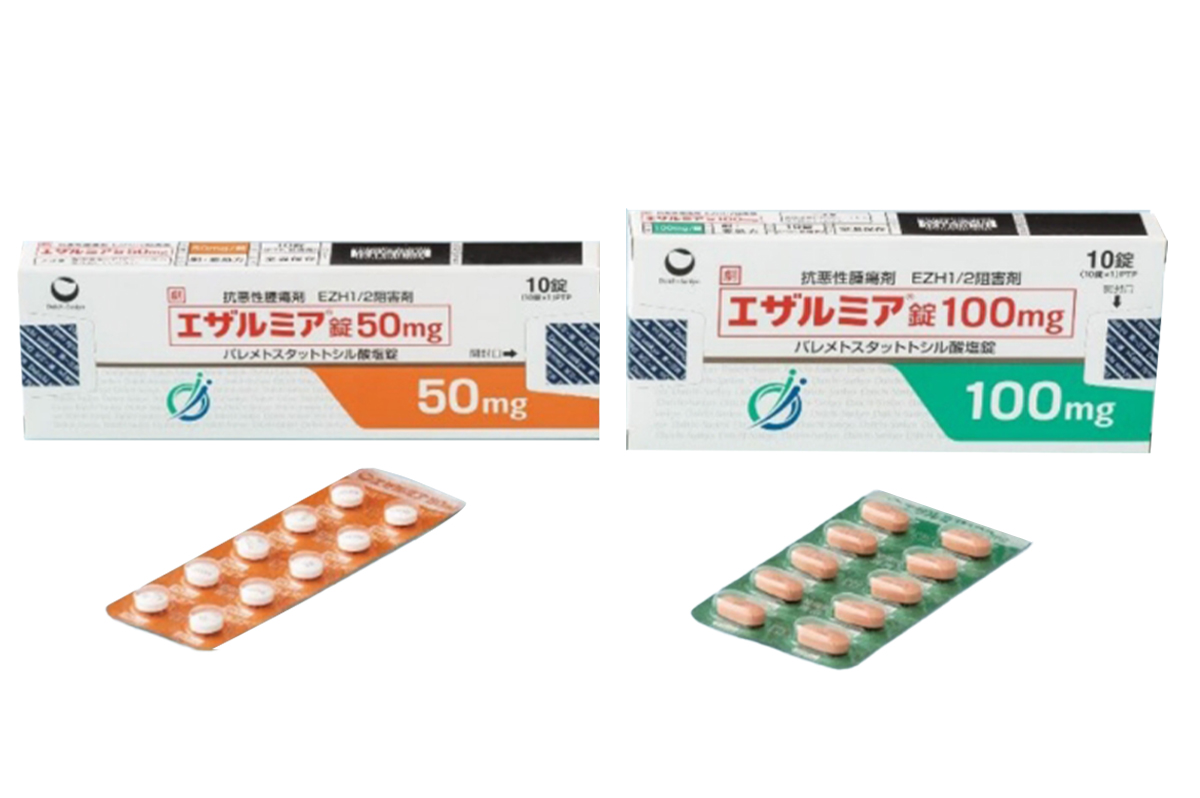
伐美妥司他是一种口服的、选择性EZH1和EZH2双抑制剂,属于组蛋白甲基转移酶抑制剂类抗肿瘤药物。通过抑制EZH1/2的活性,降低组蛋白H3K27的甲基化水平,抑制肿瘤细胞的增殖。适用于特定类型的复发或难治性T细胞淋巴瘤。
药品称呼
通用名称:伐美妥司他、Valemetostat
商品名称:Ezharmia
适应靶点
EZH1/2(组蛋白甲基转移酶EZH1和EZH2)
适应症和适应人群
适应症:复发或难治性成人T细胞白血病淋巴瘤(ATLL);复发或难治性外周T细胞淋巴瘤(PTCL)。
适应人群:成人患者,经病理诊断确认,且既往治疗失败或不适用其他治疗方案。
规格与性状
规格:50mg*10片/盒,100mg*10片/盒。
性状:50mg片为白色薄膜衣片,直径约8.1mm,重量约220mg;100mg片为红白色椭圆形薄膜衣片,长径约14.1mm,短径约6.7mm,重量约440mg。
主要成分
活性成分:帕美妥司他托西酸盐
辅料:结晶纤维素、交联羧甲基纤维素钠、淀粉甘醇酸钠、轻质无水硅酸、硬脂酸镁、羟丙甲纤维素、滑石粉、二氧化钛。100mg片额外添加:黄色氧化铁、红氧化铁。
用法用量
常规剂量
成人推荐剂量为200mg(以帕美妥司他计),每日一次,空腹口服。需在餐前1小时或餐后2小时服用,以避免食物影响吸收。
剂量调整
根据患者耐受性进行个体化剂量调整,最低可调整至50mg每日一次。若50mg仍无法耐受,应终止治疗。
剂量调整标准(根据不良反应)
血液学毒性(如中性粒细胞减少、血小板减少、贫血):根据严重程度暂停给药,恢复后按原量或降低一个剂量级别重新开始。
非血液学毒性(≥3级):暂停给药至恢复至≤1级或基线水平,恢复后按原量或降低一个剂量级别继续治疗。
与CYP3A或P-gp抑制剂合用时的剂量调整:与强CYP3A抑制剂或P-gp抑制剂合用时,需将伐美妥司他剂量降至100mg或50mg。与兼具强CYP3A和P-gp抑制作用的药物合用时,应避免使用伐美妥司他或降至50mg。
具体您可以阅读伐美妥司他完整用法用量信息,建议在医生的指导下正确用药。推荐文章:伐美妥司他的用法用量。
不良反应
常见不良反应(发生率≥10%)
血液系统:血小板减少(48.4%)、贫血(28.4%)、中性粒细胞减少(21.8%)、白细胞减少(13.3%)。
皮肤:脱发(20%以上)、皮疹(10–20%)、皮肤干燥(<10%)。
消化系统:恶心、腹泻。
其他:味觉障碍(31.6%)、疲劳、食欲减退、发热、外周性水肿。
严重不良反应
骨髓抑制(需定期监测血常规)、感染(包括上呼吸道感染、耶氏肺孢子菌肺炎)、二次恶性肿瘤(如急性髓系白血病、骨髓增生异常综合征)。
具体您可以阅读伐美妥司他完整副作用信息,建议在医生的指导下正确用药。推荐文章:伐美妥司他的副作用。
注意事项
用药前需充分告知患者疗效与风险,获取知情同意。
必须在具备紧急处理条件的医疗机构,由经验丰富的医师监督下使用。
定期监测血常规,及时发现和处理骨髓抑制。
避免与食物同服,以保障吸收效率。
注意药物相互作用,尤其与CYP3A/P-gp抑制剂或诱导剂合用时需调整剂量。
PTP包装需取出后服用,避免误吞铝箔导致食管损伤。
特殊人群用药
【孕妇】仅在对母体益处大于胎儿风险时使用。动物实验显示胚胎毒性和致畸性。
【哺乳期女性】建议停止哺乳。动物数据显示药物可经乳汁排泄。
【具有生殖潜力的男性和女性】女性在用药期间及停药后2周内需采取有效避孕。男性需使用避孕套,避免通过精液影响胎儿,且可能影响精子生成。
【儿童使用】目前尚未开展以儿童为研究对象的临床试验,儿童使用本药的安全性和有效性尚未得到证实,暂不推荐儿童使用。
【老年人使用】说明书中尚未明确。
【肾功能损害】说明书中尚未明确。
【肝功能损害】重度肝功能损害患者无临床数据,需谨慎使用。轻中度肝功能损害患者无需调整剂量。
禁忌症
对伐美妥司他任何成分过敏者禁用。
药物相互作用
1.强CYP3A/P-gp抑制剂
使用强CYP3A或P-gp抑制剂会升高伐美妥司他血药浓度。临床使用中伐美妥司他需减量,并密切监测不良反应。
2.中效CYP3A抑制剂
使用中效CYP3A抑制剂可能升高伐美妥司他浓度。临床建议应密切监测不良反应。
3.强/中效CYP3A诱导剂
使用强或中效CYP3A诱导剂会降低伐美妥司他血药浓度。可考虑更换为无或弱CYP3A诱导作用的药物。
4.P-gp底物药物
伐美妥司他抑制P-gp,可能升高合用药物的血药浓度。应监测合用药物的不良反应,例如地高辛和非索非那定。
药物过量
说明书中尚未明确。
药代动力学
吸收:口服后Tmax约为2–5小时,高脂肪餐可使Cmax和AUC降低50%以上。
分布:血浆蛋白结合率94–95%,主要与α-1酸性糖蛋白结合。
代谢:主要经CYP3A代谢,生成活性代谢物CAIZ-1809a。
排泄:主要经粪便排泄(79.8%),尿中排泄15.6%,半衰期约20小时。
特殊人群:轻中度肝损伤患者无需调整剂量。
贮存方法
室温保存,避免潮湿。有效期3年。
生产厂家
日本第一三共株式会社