



STELLAR 试验(NCT04576988)评估了索特西普(Sotatercept)在 PAH 成年患者中的疗效。STELLAR 是一项全球性、双盲、安慰剂对照、多中心、平行组临床试验,323 名 PAH 患者(WHO 第 1 FC II 或 III 组)按 1:1 随机分配到索特西普(Sotatercept)(目标剂量 0.7毫克/千克)(n=163)或安慰剂(n=160),每 3 周皮下注射一次。
参与者中79%为女性;年龄中位数为 48 岁(范围:18 至 82 岁),体重中位数为 68 千克(范围:38 至 141 千克);89% 为白人/高加索人,2% 为黑人/非洲裔美国人,2% 为亚洲人,0.3% 为美国印第安人或阿拉斯加原住民,0.3% 为夏威夷原住民或其他太平洋岛民,6% 为失踪/其他种族。最常见的 PAH 病因是特发性 PAH(59%)、遗传性 PAH(18%)和与结缔组织病 (CTD) 相关的 PAH(15%)。STELLAR 排除了人类免疫缺陷病毒(HIV)相关 PAH、门静脉高压相关 PAH、血吸虫病相关 PAH 和肺静脉闭塞性疾病患者。从 PAH 诊断到筛查的平均时间为 8.8 年。大多数参与者正在接受三种(61%)或两种(35%)治疗 PAH 的背景药物,40% 正在接受前列环素输注。患者的基线WHO FC为II级(49%)或III级(51%)。
主要疗效终点是第24周时6分钟步行距离(6 MWD)与基线相比的变化。在索特西普(Sotatercept)组中,经安慰剂调整后的 6 分钟步行距离中位数增加了 41 米(95% CI:28,54;p<0.001)。下图显示了相关亚组在第 24 周经安慰剂调整后的 6 MWD 变化情况。
图:第 24 周时各分组的 6 分钟步行距离(米)与基线相比的变化情况
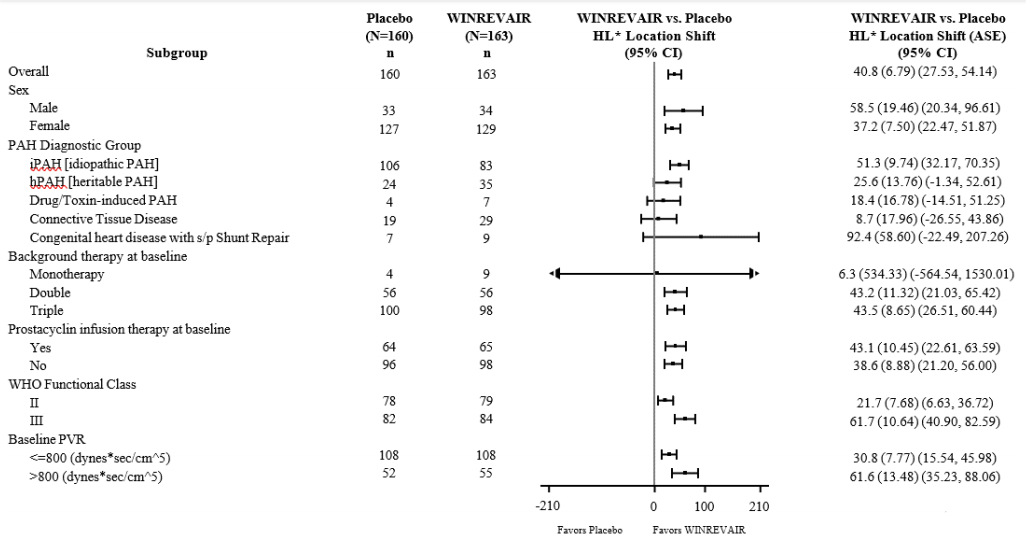
*与安慰剂估计值相比的霍奇斯-莱曼估计位置偏移(所有配对差异的中位数)。ASE = 渐进标准误差
死亡受试者在第 24 周时的 6 MWD 与基线相比的变化归因于-2000 米,以获得最差排名。由于非致死性临床恶化事件而导致数据缺失的受试者,其第 24 周时的 6 MWD 与基线相比的变化被估算为-1000 米,以获得次差排名。
接受索特西普(Sotatercept)治疗的患者中,有 29% 在第 24 周时比基线值提高了至少 1 个 WHO FC,而接受安慰剂治疗的患者中只有 14%(p<0.001)。
与安慰剂相比,使用索特西普(Sotatercept)治疗可使任何原因导致的死亡或 PAH 临床恶化事件减少 84%(见下表和图)。这些结果一直记录到最后一名患者完成第 24 周访视为止(数据截止到数据截止点;中位暴露持续时间为 33.6 周)。
表:任何原因引起的死亡或PAH临床恶化事件
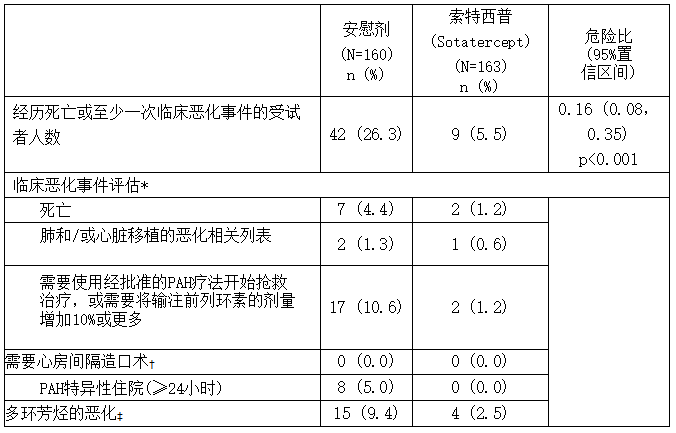
* 一个受试者的临床恶化情况可以有不止一次的评估记录。
† 没有发生过心房隔膜切除术。
‡ PAH恶化定义为与基线值相比,在任何时间发生的以下两种事件,即使它们开始于不同时间:(a)世卫组织功能分级恶化(II至III、III至IV、II至IV等)。);和(b)6 MWD下降≥15%(由两个6 MWTs间隔至少4小时但不超过一周证实)。
N =该类别中的受试者人数。
6 MWT = 6分钟步行试验。
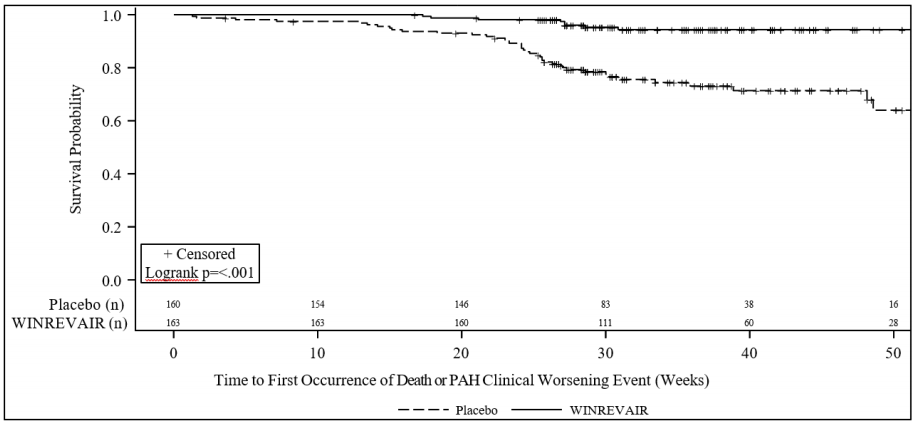
图:死于任何原因或首次出现 PAH 临床恶化事件的时间 Kaplan-Meier 图



互联网药品信息服务资格证书

孟加拉耀品国际授权书

孟加拉珠峰制药授权书

孟加拉伊思达制药授权书

孟加拉伊思达制药授权书

土耳其医院授权书
 正品保障
正品保障
 厂家直采
厂家直采
 专业药师
专业药师
 品类齐全
品类齐全