



向患者输注之前,应将制备好的注射用舒巴坦钠(XACDURO)溶液置于室温环境中(超过15至30分钟)。通过静脉(IV)输注方式,在3小时内使用所有剂量的XACDURO。
XACDURO是一种共包装试剂盒,含有1个透明的单剂量小瓶舒巴坦1g和2个琥珀色的单剂量小瓶达洛巴坦0.5g无菌粉末,必须在静脉输注前使用无菌技术重新配制和进一步稀释。
XACDURO不含抑菌防腐剂,制备的溶液必须在2°C至8°C(36°F至46°F)冷藏条件下储存24小时后才能使用,丢弃未使用的部分。

XACDURO试剂盒(包括一个舒巴坦1 g单剂量小瓶和两个度洛巴坦0.5 g单剂量小瓶)、100 mL输液袋,内含0.9%氯化钠注射液,USP、10 mL无菌注射用水,USP、10 mL无菌注射器和酒精湿巾。

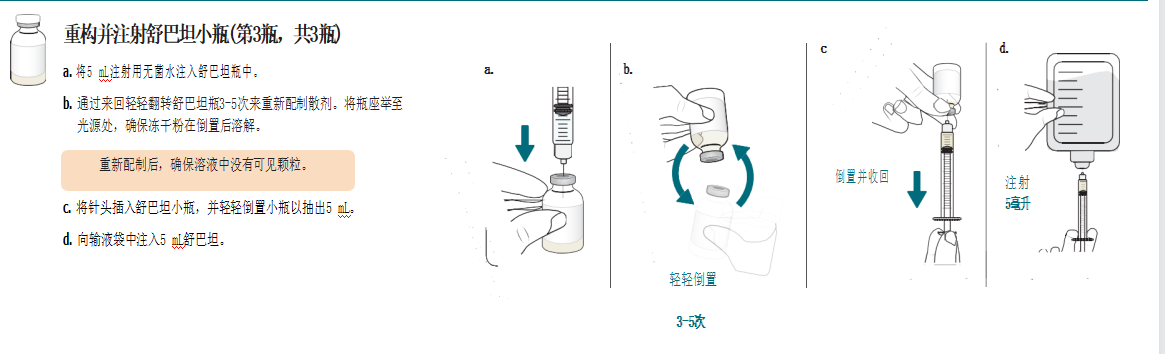
1、 用5mL注射用无菌水重新配制舒巴坦1 g单剂量小瓶,并轻轻摇晃以使其溶解。每个重新配制的小瓶中每5 mL透明、无色至微黄色溶液含1 g舒巴坦。重新配制的溶液不能直接注射,必须在静脉输注前稀释。稀释必须在重建后1小时内进行。
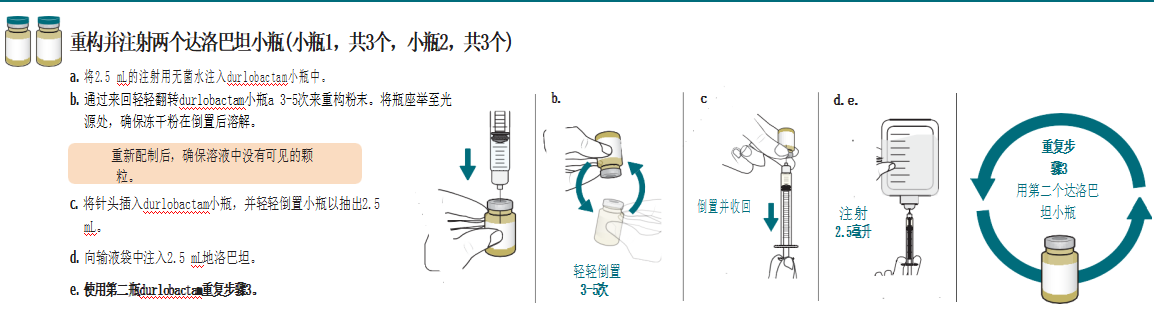
2、用2.5 mL的注射用无菌水重新配制每个dur lobatam 0.5g单剂量小瓶,并轻轻摇晃以使其溶解。每个重新配制的药瓶中,每2.5 mL透明、浅黄色至橙色溶液中含有0.5 g的硬叶ctam。重新配制的溶液不能直接注射,必须在静脉输注前稀释。稀释必须在重建后1小时内进行。
3、为制备所需的XACDURO剂量,抽取5 mL重构舒巴坦和5 mL(每瓶2.5 mL)重构达洛巴坦。将抽出量的舒巴坦和达洛巴坦加入100 mL的0.9%氯化钠注射液(USP)输液袋中。丢弃未使用的部分。
在溶液和容器允许的情况下,应在给药前目视检查肠胃外药物产品是否存在颗粒物质和变色。制备的XACDURO溶液应为透明、浅黄色至橙色溶液,无微粒。如果XACDURO溶液混浊或含有微粒,请勿使用。

将制备好的袋在2°C至8°C(36°F至46°F)的温度下储存在冰箱中,直至使用。从开始重新配制粉末到输注结束之间的时间不应超过24小时,不要冷冻。
相关热文推荐:注射用舒巴坦钠说明书?
注:文章信息来源于网络,仅供医护人员内部讨论,不作为用药依据,具体用药指引,请咨询主治医师。
