替沃扎尼(Tivozanib)是一种口服激酶抑制剂,用于治疗特定条件下的成人患者。以下内容是根据说明书整理的本药品的适应症、用法用量、不良反应及注意事项等信息,仅供参考。请务必严格遵循医嘱使用。
药品称呼
通用名称:替沃扎尼、Tivozanib
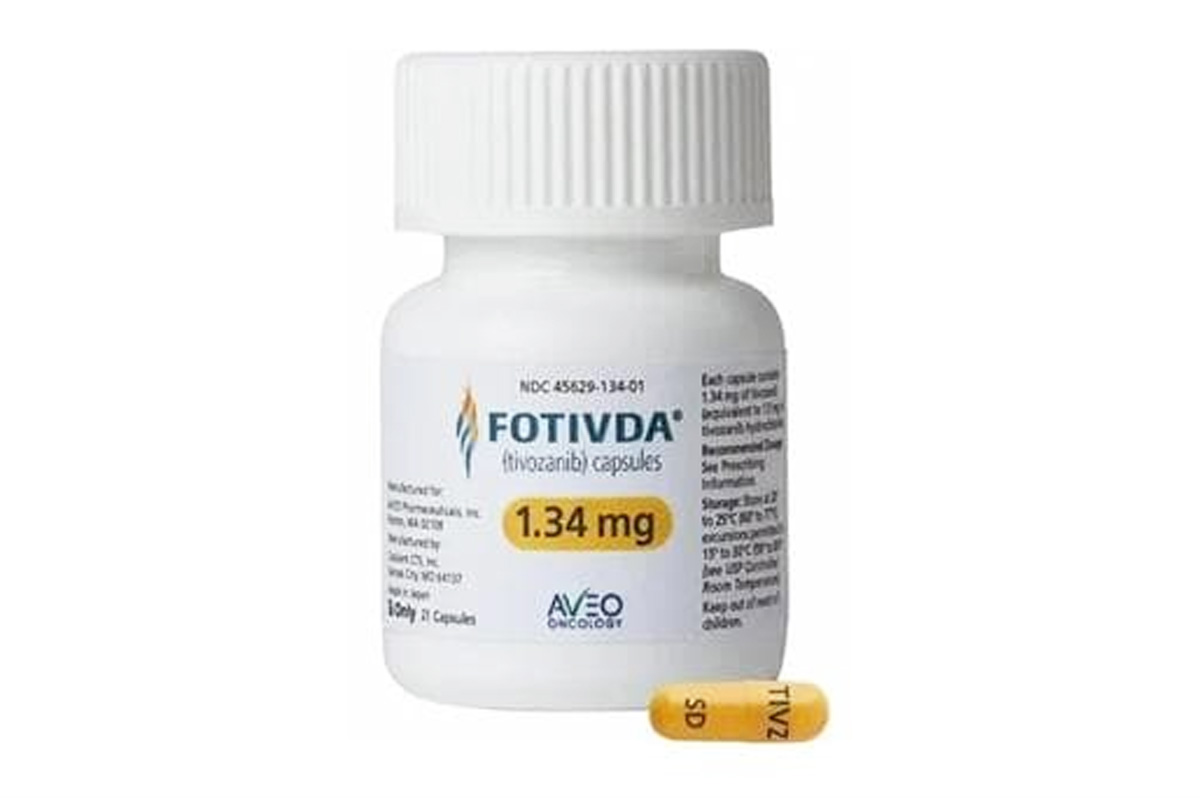
商品名称:Fotivda
适应靶点
替沃扎尼是一种酪氨酸激酶抑制剂,主要作用于血管内皮生长因子受体(VEGFR)-1、VEGFR-2和VEGFR-3。
适应症和适应人群
用于治疗接受过两种或更多种先前全身治疗后复发或难治性晚期肾细胞癌(RCC)的成人患者。
规格与性状
规格
1.34mg*21粒/盒。
性状
1.34mg胶囊:亮黄色不透明胶囊体,胶囊盖印有深蓝色“TIVZ”字样,胶囊体印有深蓝色“SD”字样。
主要成分
活性成分:替沃扎尼盐酸盐。
辅料:甘露醇、硬脂酸镁等。
用法用量
1、推荐剂量
推荐用量替沃扎尼1.34mg,每日一次,连续服用21天,然后停药7天(28天一个周期),直至疾病进展或出现不可接受的毒性。
2、剂量调整
根据不良反应情况可能需要中断剂量或减少剂量。对于中度肝功能损害患者,剂量应减少至0.89mg。
3、给药方式
口服,有无食物均可。整粒吞服,不要打开胶囊。
具体您可以阅读替沃扎尼完整用法用量信息,建议在医生的指导下正确用药。推荐文章:替沃扎尼(Tivozanib)的用法用量。
不良反应
常见不良反应(≥20%)
疲劳、高血压、腹泻、食欲减退、恶心、发音困难、甲状腺功能减退、咳嗽和口腔炎。
常见3级或4级实验室异常(≥5%)
钠降低、脂肪酶升高和磷酸盐降低。
具体您可以阅读替沃扎尼完整副作用信息,建议在医生的指导下正确用药。推荐文章:替沃扎尼(Tivozanib)的副作用。
注意事项
高血压和高血压危象:治疗前控制血压,治疗期间监测血压。
心脏衰竭:监测心脏衰竭的症状和体征。
心脏缺血和动脉血栓栓塞事件:密切监测有风险的患者。
静脉血栓栓塞事件:密切监测有风险的患者。
出血事件:密切监测有出血风险或出血史的患者。
蛋白尿:监测蛋白尿,根据情况调整剂量或中断治疗。
胃肠道穿孔和瘘管形成:监测症状,严重情况下永久停药。
甲状腺功能异常:监测甲状腺功能。
伤口愈合受损:择期手术前至少停药24天,重大手术后至少2周内不使用,直至伤口充分愈合。
可逆性后部白质脑病综合征(RPLS):出现症状时停药。
胚胎-胎儿毒性:可能对胎儿造成伤害,建议育龄期女性和男性采取有效避孕措施。
对酒石黄的过敏反应:0.89mg胶囊含有FD&CYellowNo.5,可能引起某些敏感患者的过敏反应。
特殊人群用药
【孕妇】替沃扎尼可能导致胎儿损伤,因此需明确告知孕妇潜在风险,并建议不推荐孕妇使用。用药前应确认有生殖潜力女性的妊娠状态。
【哺乳期女性】目前没有数据表明替沃扎尼是否会分泌到人乳中,也不清楚其对哺乳婴儿或母乳分泌的影响。鉴于潜在的严重不良反应风险,建议哺乳期女性在用药期间及末次剂量后1个月内避免母乳喂养。
【具有生殖潜力的男性和女性】用药前需要确认有生殖潜力女性的妊娠状态,并采取有效的避孕措施。对于有生殖潜力的女性及其伴侣的男性,在用药期间及末次剂量后1个月均需使用避孕措施。此外,替沃扎尼可能影响生育能力,患者应在治疗前被告知这一风险。
【儿童使用】替沃扎尼在儿科患者中的安全性和有效性尚未得到证实,因此不建议在儿童中使用该药物。
【老年人使用】根据现有数据,无需根据年龄调整替沃扎尼的剂量,老年患者(≥65岁)与年轻患者相比,在安全性或有效性上未观察到显著差异。
【肾功能损害】轻度至重度肾功能损害患者(肌酐清除率15-89mL/min)无需调整替沃扎尼的剂量;然而,对于终末期肾病患者的推荐剂量尚未确定。
【肝功能损害】轻度肝功能损害患者无需调整剂量;中度肝功能损害患者应按照特定周期调整剂量;而对于重度肝功能损害患者,由于缺乏足够的数据支持,推荐避免使用替沃扎尼,或至少在其剂量尚未确定的情况下谨慎使用。
禁忌症
替沃扎尼无特定禁忌症列出。
药物相互作用
其他药物对替沃扎尼的影响
替沃扎尼主要经细胞色素P4503A4(CYP3A4)代谢。与强效CYP3A诱导剂合用时,会降低替沃扎尼的暴露量,可能削弱其抗肿瘤活性,因此应避免两者合用。
药物过量
可能导致严重高血压和高血压危象,甚至死亡。无特定解毒剂,应密切监测血压和其他潜在不良反应,提供支持性治疗。
药代动力学
吸收:中位Tmax为10小时,范围3至24小时。
分布:表观分布容积为123L,蛋白结合率≥99%。
消除:表观清除率为0.75L/h,半衰期为111小时。
代谢:主要由CYP3A4代谢。
排泄:79%通过粪便排泄,12%通过尿液排泄。
贮存方法
储存于20℃至25℃环境下,允许在15℃至30℃之间进行短期偏移;需置于儿童不易触及处,防止误服。
研发公司
美国AVEO制药