



1、局部晚期/转移性非小细胞肺癌
在两项随机对照临床试验中评价了安罗替尼单药用于局部晚期/ 移性非小细胞肺癌的有效性。
ALTER0303是一项多中心、随机双盲、安慰剂平行对照的Ⅲ期临床试脸,纳入了437例经过至少两种系统化疗后失败(EGFR突变和 ALK阳性的患者还需接受过相应的靶向药物治疗后进展)的晚期/转移性非小细胞肺癌患者。主要研究终点为总生存期(0S) ,次要终点包括无进展生存期(PFS)和客观缓解率(ORR) 。患者按2:1随机分为两组:试验组给予安罗普尼12毫克,每日一次,连服2周停药1周 (n=294);对照组给予安慰剂(n=143)。
437例受试者中,55.6%为60岁以下;65.2%为男性;20.1%为 ECOG评分0分,79.3%为1分;5.0%为ⅢB期,94.5%为Ⅵ期; 76.9%为腺痛,19.7%为鳞癌或腺鳞癌,3.4%为其它亚型;31.6%的患者具有 EGFR突变,1.6%为ALK阳性,96.4%的基因突变阳性患者接受了相应靶向治疗;52.9%接受了两种系统化疗方案治疗,43.0%接受了三种及以上系统化疗方案治疗;41.9%既往接受过放疗。两组的基线性别、年龄、分期、ECOG评分、组织学类型、基因突变状态、既往治疗史具有可比性。安罗普尼组中位治疗时间为6个周期,安慰剂组中位治疗时间为2个周期。
研究在发生了292例生存事件(66.8%)时对主要终点进行了有效性分析。安罗普尼组中位总生存期为9.5月(95%CI为8.1~10.5),安慰剂组为6.4月(95%CI为4.9~8.0),安罗普尼组中位总生存期较安慰剂组延长,风险比(HR)为0.70, 95%CI为0.55~689, p=0,002,对比安慰剂,安罗普尼降低了30%的死亡风险。接受安罗普尼治疗的患者1年生存率为39.5%,安慰剂组为27.8%主要有效性数据见表5。
表5:ALTER0303的主要有效性结果(FAS)
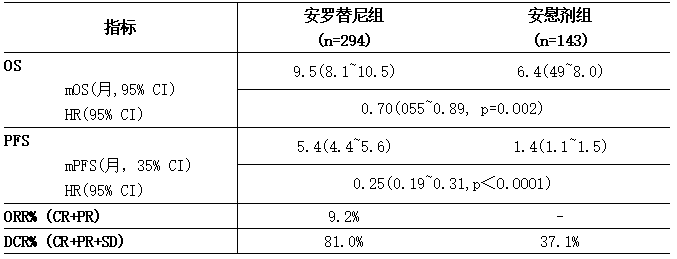
注:每月按30.4天计;
FAS:全分析集;mOS:中位总生存期;mPFS:中位无进展生存期;CR:完全缓解;PR:部分缓解;SD:疾病稳定;ORR:客观缓解率;DCR:疾病控制率。
图:ALTER0303两组生存期(OS,月)疗效对比(FAS集)
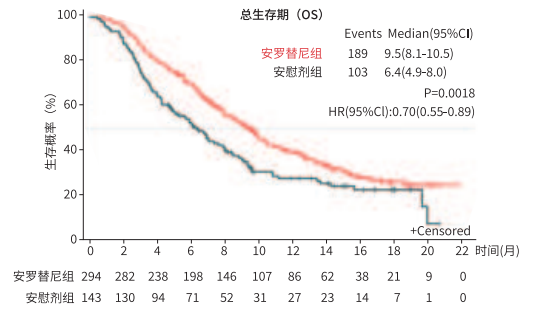
基于EGFRS因突变状态的亚组分析
在ALTER0303研究中,31.6% (138/437)的患考为EGFR突变阳性,阳性患者和阴性患者均观察到了OS的获益。在ALTER0302研究中EGFR突变阳性(21例)和阴性或状态不明亚组(96例)也观察到了一致获益趋势,表6列出了ALTER0303试验EGF理变患者的亚组分析数据。
表6:ALTERO303研究中EGFR突变亚组的疗效结果
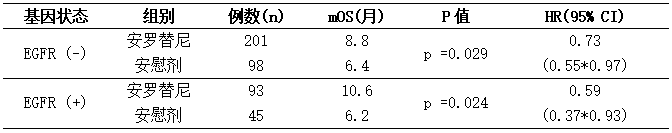
注:每月按30.4天计。
在ALTER0303研究中未对EGFR突变阳性患者接受既往靶向药物治疗后进展的患者,检测T790M耐药突变,针对T790M阳性患者的获益尚需进一步研究证实。安罗替尼针对该人群的研究正在进行中。
2、晚期软组织肉瘤
在两项临床试验中评价了安罗替尼胶囊治疗转移性软组织肉瘤的有效性。
ALTER0203研究是一项多中心、随机双盲、安慰剂对照的确证性临床试验,纳入233例具有可测量病灶、既往至少接受过含蒽环类化疗方案治疗后进展或复发(腺泡状软组织肉瘤、透明细胞肉瘤除外)的转移性软组织肉瘤患者。本项研究纳入滑膜肉瘤、平滑肌肉瘤、腺泡 状软组织肉痛、未分化多形性肉瘤/恶性纤维组织细胞瘤、脂肪肉瘤、 纤维肉瘤、透明细胞肉瘤、上皮样肉瘤共8个亚型;其中158例患者, 服用安罗替尼12毫克,连用二周停药一周治疗,对照组75例。
盐酸安罗替尼组有效性结果见表7、表8和图2。
表7:ALTER0203研究有效性结果(FAS集)
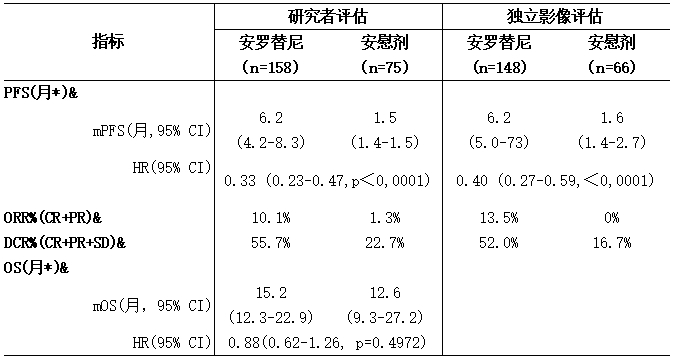
*:每月按30.4天计;&:截止2017年4月30日;#:截止2018年4月30日.
FAS:全分析集;mPFS:中位无进展生存期;CR:完全缓解;PR:部分缓解;SD:疾病稳定;ORR:客观缓解率;DCR:疾病控制率
表8:ALTER0203研究各病理亚型客观缓解率(%, FAS集)
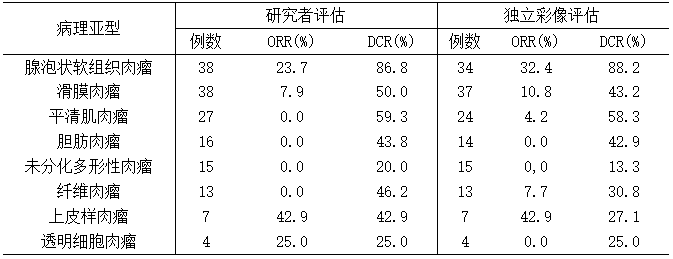
ORR:客观缓解率;DCR:疾病控制率。
图:ALTER0203研究无进展生存Kaplan-Meier曲线(PFS,月)(FAS)
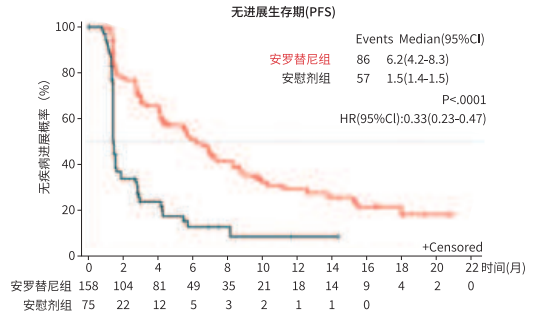
3、小细胞癌症
在一项随机对照临床试验中评价了安罗替尼单药治疗小细胞肺癌的有效性。
ALTER1202是一项多中心、随机、双盲、安慰剂平行对照的Ⅱ期临床试验,纳入119例具有可测量病灶、既往至少接受过2种化疗方案治疗后进展或复发的小细胞肺癌患者,其中安罗普尼组81例。
119例患者中,ECOG评分0分占5.9%, 85.7% 1分,8.4% 2分; 10.9%为局限期,89.1%为广泛期。其中25.2%的患者基线伴脑转移; 76.5%患者既往接受了2种系统化疗方案治疗,23.5%接受超过2种, 71.4%既往接受过放疗。两组患者的基线均衡可比,安罗替尼组中位治疗时间4.6个周期;安慰剂组1.6个周期。
截止2018年6月30日,安罗普尼组中位无进展生存期4.1月(95% CI: 2.8-4.2), 安慰剂组 0.7月(95% Cl: 0.7-68) , 肿瘤复发风险
(HR)降低80.8%,差异有显著统计学意义(HR=0.192, 95%CI: 0.117-0.315, p< 0.0001)
安罗普尼组和安慰剂组的中位总生存期分别为7.3月(95%CI: 6.5-10.5)和4.9月(95%CI:2.6-6.7),死亡风险(HR)降低47.2%,差异有统计学意义(HR=0.528, 95%CI为0.304-0.918, p=0.0210) 。主要有效性结果见表9、图3。
表9:ALTER1202的主要有效性结果(FAS)
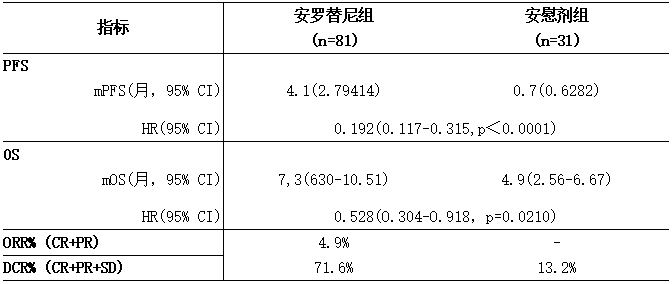
注:每月按30.4天计;
FAS:全分析集;mPFS:中位无进展生存期;mOS:中位总生存期;CR:完全缓解;PR:部分缓解;SD:疾病稳定;ORR:客观缓 解率;DCR:疾病控制率。
图:ALTER1202研究无进展生存Kaplan-Meier曲线(PFS;月)(FAS)
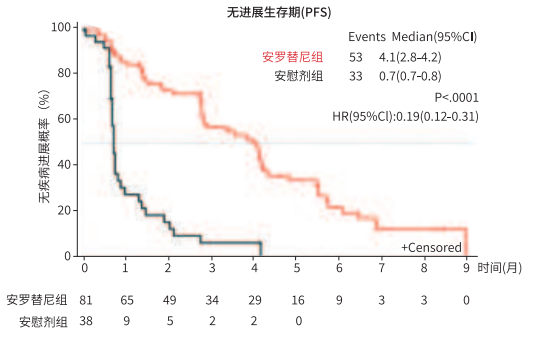
安罗替尼在广泛期小细胞肺癌中的确证性试验正在进行中.
4、局部晚期/转移性甲状腺髓样癌
在两项临床试验中评价了安罗替尼单药用于局部晚期/转移性甲状 腺髓样癌的有效性。
ALTER01031是一项多中心、随机、双盲、安慰剂平行对照的关键临床试验,纳入91例具有可测量病灶、无法手术的局部晚期或转移性甲状腺髓样癌患者,其中安罗替尼组62例。
截止2018年9月30日,安罗普尼组中位无进展生存期20.7月 (95%CI: 14.03-34.63),安慰剂组11.1月(95%CI: 5.82-14.32),肿瘤复发风险(HR)降低47%,若异有显著统计学意义(HR=0.53, 95%CI: 0.30-0.95, p=0.0289)。本试验允许交叉,截止统计日期, 两组的中位总生存期均未获得。主要有效性结果见表10、图4。
表10:ALTER01031的主要有效性结果(FAS)
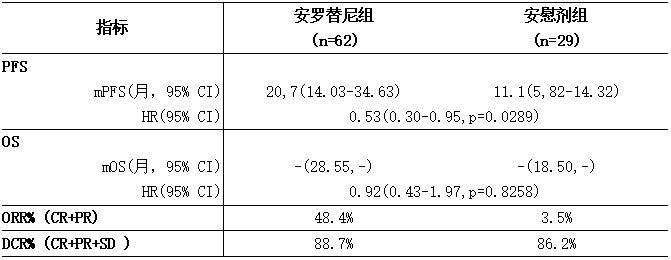
注:每月按30.4天计;
FAS:全分析集;mPFS:中位无进展生存期;mOS:中位总生存 期;CR:完全缓解;PR:部分缓解;SD:疾病稳定;ORR:客观缓解率;DCR:疾病空置率。
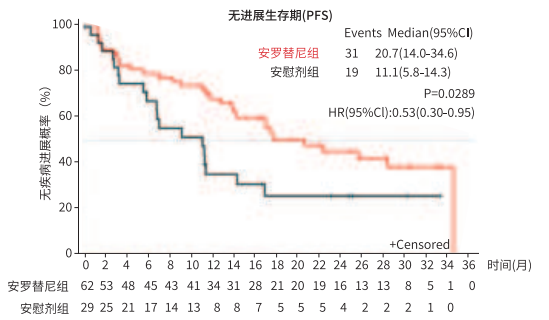
图:ALTER01031 研究无进展生存Kaplan-Meier曲线(PFS,月)(FAS)
进展性、局部晚期或转移性放射性碘难治性分化型甲状腺癌
在一项随机对照临床试验中评价了安罗替尼单药治疗局部晚期或转移性放射性碘难治性分化型甲状腺癌的有效性。试验纳入113例具有可测量 病灶、无法手术的放射性碘难治的局部晚期或转移性分化型甲状腺相患者,其中安罗普尼组76例。
截止2020年1月1日,安罗替尼组中位无进展生存期40.5月(95% CI: 28.29,-),安慰剂组8.4月(95% CI: 5.59-13.80),肿瘤复发风险 (HR)降低79%,差异有显著统计学意义(HR = 0.21; 95%CI: 0.12-0.37, p<0.0001)。本试验允许交叉,不考虑后续24例安慰组患者进展后使用安罗替尼治疗的干扰,安慰组中位OS为52.8月(95%CI: 24.81,-) ,试验组OS尚未达到(95%CI: 50.73,-) ,试验组OS有获益趋
势(HR=0.57, 95%CI: (0.29-1.12) , p =0.0976),主要有效性结果见表11、图5。
入组前12个月内有影像学进展的共91例,其中安罗替尼62例;入组前12个月内有影像学进展,同时满足TSH抑制剂治疗下TSH≤0.5mlU/升, 和放射性碘难治【定义为(1)病灶不具有碘亲和性:低碘饮食、充分 TSH升高(≥30mlU/升)条件下RAI扫描后证实不存在RAI摄取、或(2)RAI积累剂量≥600mCi或22GBq且距离入组至少间隔3个月、或(3)虽然 RAI治疗时存在碘-131亲和性,但放射学检查证实RAI治疗后的12个月内出现疾病进展】的有74例,其中安罗替尼组54例。针对以上2类人群进行疗效分析,提示安罗替尼较安慰剂在PFS、OS、ORR与整体人群获益趋势一 致,且存在统计学差异,见表12。
表11:ALTER01032的主要有效性结果(FAS)
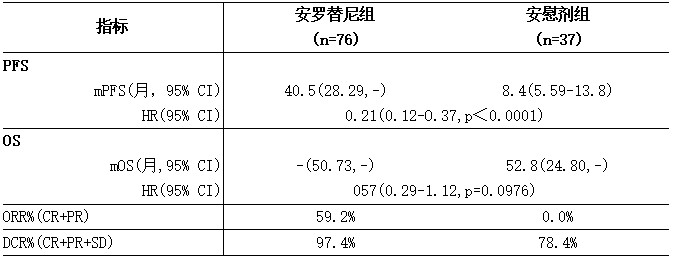
图:安罗替尼治疗分化型甲状腺癌无进展生存Kaplan-Meier曲线(PFS,月)(FAS)
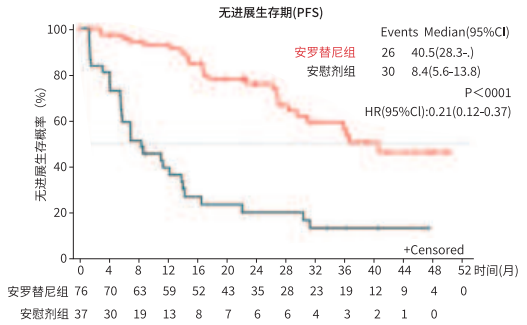
表12:ALTER01032的主要有效性结果在特定患者人群的疗效分析(FAS)
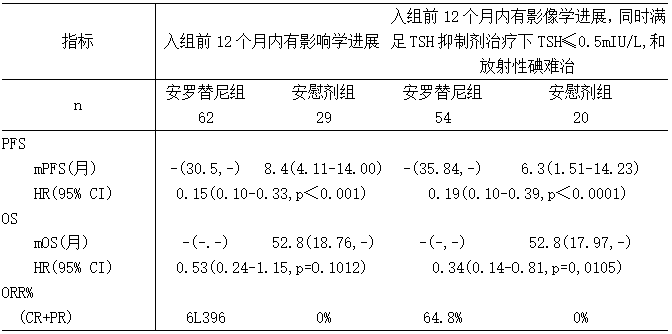
注:每月按30.4天计;
FAS:全分析集;mPFS:中位无进展生存期;mOS:中位总生存 期;CR:完全缓解;PR:部分始解;ORR:客观缓解率。



互联网药品信息服务资格证书

孟加拉耀品国际授权书

孟加拉珠峰制药授权书

孟加拉伊思达制药授权书

孟加拉伊思达制药授权书

土耳其医院授权书
 正品保障
正品保障
 厂家直采
厂家直采
 专业药师
专业药师
 品类齐全
品类齐全