



本说明书描述了在临床试验中观察到的判断为可能由安罗替尼引起的不良反应及其发生率。不良反应包括由研究者判定为与安罗替尼肯定有关、很可能有关、可能有关、可能无关以及无法判定的不良事件。由于各临床试验不是在相同条件下开展,一个临床试验中观察到的不良反应发生率与其他临床试验观察到的不良反应发生率不宜直接比较,也未必能准确预测临床实践中的真实发生率。
1、安全性特征
总结了安罗替尼已开展的23项临床试验总计1888例晚期肿瘤患者的不良反应数据,覆盖了非小细胞肺癌、软组织肉瘤、小细胞肺癌和甲状腺髓样癌等实体瘤患者。这些患者起始口服安罗替尼的剂量为12毫克,连服2周,停药1周。发生率≥10%的不良反应有:高血压、疲乏、手足综合征、高甘油三酯血症、蛋白尿、腹泻、食欲下降、血促 甲状腺激素升高、高胆固醇血症、甲状腺功能减退症等。
2、不良反应汇总表
表3汇总了这23项安罗替尼临床试验,观察1888例患者的不良反应发 生情况,并按照系统器官分类和发物率列出。发生频率分为:十分常见 (≥10%),常见(1%~10%,含1%),偶见(0.1%~1%,含0.1%) ,罕见(0.01%~0.1%,含0.01%) ,十分罕见(<0.01%) 。在每个发生频率分组内,按严重程度从高到低依次列出这些不良反应。
表3:使用安罗替尼患者的不良反应发生情况
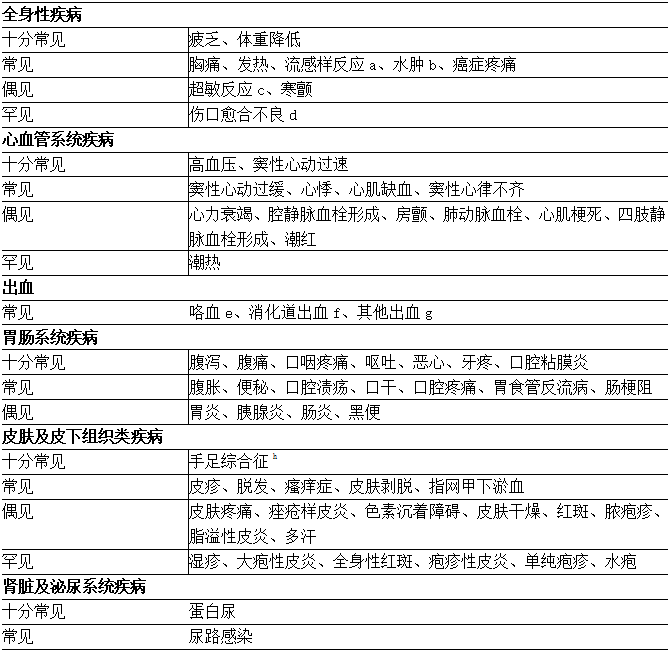
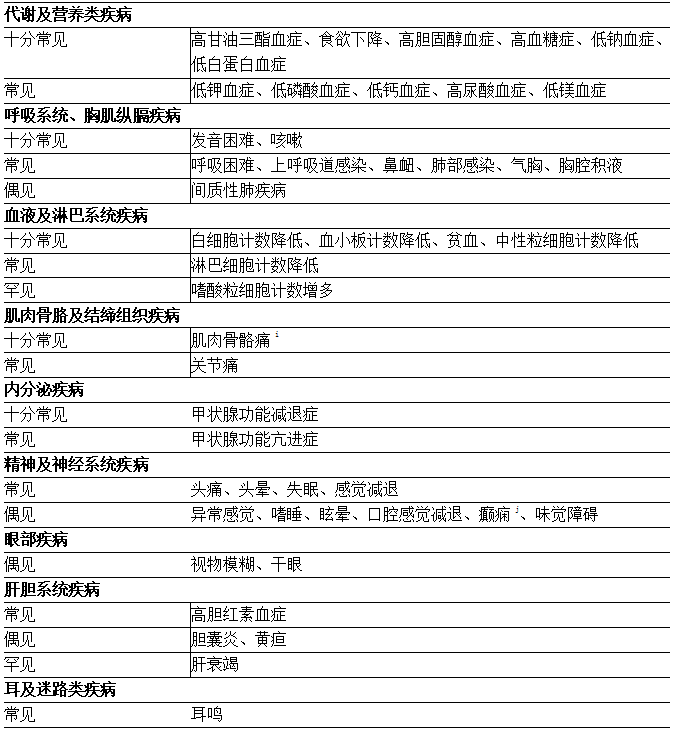

a流感样反应主要表现为寒颤、鼻塞、流鼻涕、肌肉酸痛、乏力等症状;
b水肿包括外周水肿、面部水肿、局部水肿、全身性水肿;
c超敏反应包括全身过敏性反应、上呼吸道超敏反应、急性过敏反应等;
d临床试验排除了存在创口未愈合的患者;
e咯血包括咯血和支气管出血等肺和上呼吸道的出血事件;
f消化道出血包括齿龈出血、口腔出血、咽部充血、胃出血、肠出 血、肛门出血、痔疮出血等;
g其它出血包括肿瘤出血、甲床出血、伤口出血、皮下出血、阴道出血、月经增多、子宫出血、视网膜出血、结膜出血和脑出血等;
h手足综合征在MedDRA中的术语为掌跖红肿综合征;
i肌肉骨骼痛包括背痛、肢体疼痛、肌痛、骨骼肌肉疼痛、颈痛、 骨痛、胸部肌肉骨骼疼痛和腰肋疼痛;
j癫痫包括部分性癫痫发作;
3、安罗替尼重要不良反应:
基于使用安罗替尼的1888例晚期肿瘤患者的安全性特征,现重点 列出以下特定的不良反应信息。
1)出血:出血是安罗替尼最重要的不良反应,各项研究共报告了142例咯血(7.5%),其中13例(0.7%)为3/4级咯血,3例(0.2%)因大咯血导致死亡。
2)其它出血事件:鼻衄88例(4.7%),其中3/4级32例(0.2%); 齿龈出血60例(3.2%) ,其中3/4级1例(0.1%);喉部出血13例(0.7%),上消化道出血15例(0.8%),其中3/4修6例(0.3%) , 2例(0.1%)死亡;下消化道出血37例(2.0%),其中3/4例(0.2%), 1例(0.1%)死亡;肺出血4例(0.2%) , 1例(0.1%)死亡;脑出血6例 (0.3%),其中3/4级4例(0.2%) , 1例(0.1%)死亡。指/趾甲下淤血变色33例(1.8%),阴道出血11例(9.6%),均为1/2级。
3)高血压:高血压是安罗替尼最常见的不良反应,各项研究共报告发 生1084例(57.4%)高血压,其中3/4级283例(15.0%)。高血压在服药后2周内出现,为持续性不随连二停一给药波动。
4)心肌缺血:各项研究共报告发生33例(1.8%)心肌缺血,其中1级31例,2级2例。包括复发性心肌缺血、急性心肌缺血和缺血性心肌病等(不包括心肌缺血的心电图)。
5)蛋白尿:各项研究共报告发生蛋白尿691例(36.6%),其中3/4级 45例(2.4%)。
6)手足综合征:各项研究共报告发生手足综合征809例(42.9%),其中3/4级84例(4.5%);手足综合征多在给药2周内出现,表现为手足掌底部位皮肤肿胀、剥落、水泡、皲裂、出血或红斑的复合表现,常伴有疼痛。
7)胃肠道反应:各项研究共报告发生腹泻664例(35.2%),其中3/4 级36例(1.9%);腹痛515例(27.3%),其中 3/4级25例(1.3%); 恶心246例(13.0%),其中3/4级2例(0.1%);呕吐253例 (13.4%),其中3/物"例(0.4%);腹胀 110例(5.8%),其中3/4 级3例(0.2%);肠梗阻27例(1.4%),其中3/4级20例(1.1%)。
8)牙龈口腔肿痛:各项研究共报告发生口腔黏膜炎220例(1L7%), 其中3/4级14例(0.7%);牙疼240例(12.7%),其中3/4级4例 (0.2%) ; 口腔溃疡72例(3.8%),其中3/4级3例(0.2%) ; 口腔疼痛33例(1.7%),均为1/2级。
9)甲状腺功能异常:各项研究共报告发生甲状腺功能减退症388例 (20.6%),其中3/4级4例(0.2%) , 13例(0.7%)因为甲状腺功能减退症而哲停/停止安罗替尼治疗;甲状腺功能亢进症43例(2.3%), 均为1/2级,未发生因甲状腺功能亢进症而暂停/停止安罗替尼治疗。血促甲状腺激素升高547例(29.0%),其中3/4级4例(0.2%)。
10)高脂血症:各项研究共报告高甘油三酯血症711例(37.7%),其中 3/4级84例(4.5%);高胆固醇血症554例(29.3%),其中3/4级9例 (0.5%);低密度脂蛋白升高298例(15.8%),其中3/4级11例(0.6%)。
11)上市后不良反应报告
安罗替尼批准后的临床使用过程中,除上文提及的不良反应报告外,还各报告1例急性胰腺炎和心脏毒性。由于这些反应尚不确定人群的大小,尚不能准确估计其发生率并确定与药物间的明确因果关系。



互联网药品信息服务资格证书

孟加拉耀品国际授权书

孟加拉珠峰制药授权书

孟加拉伊思达制药授权书

孟加拉伊思达制药授权书

土耳其医院授权书
 正品保障
正品保障
 厂家直采
厂家直采
 专业药师
专业药师
 品类齐全
品类齐全