



上周,帕妥珠单抗(商品名:帕捷特)在中国获批用于HER2阳性晚期乳腺癌患者的一线治疗!
该方案的获批,将为HER2阳性晚期乳腺癌患者带来更久的生存获益,这将有助于实现乳腺癌诊疗的慢病化管理,使晚期乳腺癌摆脱“绝症”成为可能!
乳腺癌是女性发病率最高的恶性肿瘤。5年生存率仅20%,总体中位生存时间仅为2~3年。
HER2又称人表皮生长因子受体-2,是重要的乳腺癌预后判断因子,HER2阳性乳腺癌约占乳腺癌的20%-30%。
对于HER2阳性乳腺癌,癌细胞内HER2基因高度表达,因此就会有太多HER2蛋白出现在这些癌细胞表面,称之为HER2蛋白过表达。HER2蛋白的过表达,就会刺激癌细胞疯狂增长,侵袭性增加,复发和转移相对较快。
所以HER2阳性乳腺癌患者具有病情进展迅速、易发生淋巴结转移、化疗缓解期短、内分泌治疗相对耐药等特点,给临床治疗带来不少的困难,患者生活质量整体偏低。
HER2 阳性的早期乳腺癌患者接受曲妥珠单抗(赫赛汀)联合化疗后,仍有约 1/4 的患者在 10-11 年后出现疾病复发或死亡,高危早期乳腺癌患者出现复发或死亡的比例更高。
批准依据: 本次帕妥珠单抗HER2阳性晚期乳腺癌一线治疗适应症获批主要是基于持续长达8年随访的CLEOPATRA国际临床研究和来自中国人群的PUFFIN研究两项研究结果。
在试验中,符合条件HER2阳性晚期转移性乳腺癌患者被分为两组,一组接受曲妥珠单抗联合多西他赛,一组在此基础上加入了帕妥珠单抗,形成双靶组:帕妥珠单抗+曲妥珠单抗联合多西他赛。
无论是看国际研究的整体结果,还是单独看中国患者的结果,结论都一样:对于HER2阳性晚期转移性乳腺癌患者,双靶组整体实现了总生存期和无进展生存期的大跨越,效果更好!
在今年的 ASCO会议上,公布的CLEOPATRA研究结果显示,帕妥珠单抗联合曲妥珠单抗双靶组的中位OS为57.1个月(接近5年!),而对照组只有40.8个月,整整提高了一年半多!
而且,在帕妥珠单抗+曲妥珠单抗双靶组中,有37%的患者达到8年生存,显著高于曲妥珠单抗组的23%。
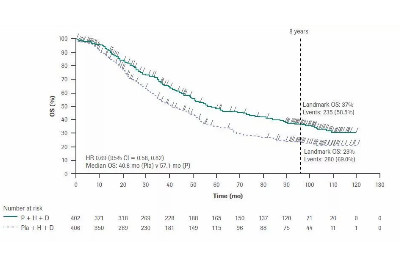
那中国患者的数据如何呢?
整体而言,PUUFFIN研究结果和CLEOPATRA的研究结果类似。在无进展生存期(PFS)获益趋势上,和全球数据保持了一致。
帕妥珠单抗联合曲妥珠单抗双靶组较对照组患者的复发和死亡风险降低了31%,目前帕妥珠单抗联合曲妥珠单抗双靶组的中位PFS为14.5个月,对照组为12.4个月。
到目前为止,国内外指南一致推荐帕妥珠单抗联合曲妥珠单抗和化疗作为HER2阳性晚期乳腺癌患者一线治疗的标准方案。
如中国医学科学院肿瘤医院徐兵河教授指出:“PUFFIN研究证实了帕妥珠单抗联合曲妥珠单抗双靶方案在中国患者身上同样具有安全性和生存获益,为中国患者更加放心地使用帕妥珠单抗联合曲妥珠单抗双靶方案提供了有力的循证医学证据。”
此次帕妥珠单抗+曲妥珠单抗+化疗三药联合获批一线疗法,有望推动国内HER2阳性晚期乳腺癌的诊疗格局变化,也证明了我国国内乳腺癌治疗逐步在与世界接轨。
近期医保谈判已尘埃落定,双靶治疗方案中的曲妥珠单抗成功通过国家医保谈判续签,且新增了新辅助治疗适应症;而帕妥珠单抗用于HER2阳性的局部晚期、炎性或早期乳腺癌患者的新辅助治疗和用于具有高复发风险HER2 阳性早期乳腺癌患者的辅助治疗也都首次被列入国家医保药品目录。
相信在国家医保政策的普及下,能够接受到规范的双靶治疗,并从中获益。
注:文章信息来源于网络,仅供医护人员内部讨论,不作为用药依据,具体用药指引,请咨询主治医师。
