Kalydeco(ivacaftor)是一种处方药,用于治疗囊性纤维化(CF)。通过靶向囊性纤维化跨膜转导调节因子(CFTR)基因上的特定突变,增强CFTR蛋白的功能,从而改善CF患者的呼吸道症状。以下是基于Kalydeco(ivacaftor)FDA说明书内容,整理出来的药品适应症、用法用量、不良反应及注意事项等。内容仅供参考,请谨遵医嘱。
药品称呼
通用名:Ivacaftor
商品名:Kalydeco
适应靶点
囊性纤维化跨膜转导调节因子(CFTR)基因上的特定突变。
适应症和适应人群
Kalydeco适用于治疗年龄在1个月及以上的囊性纤维化患者,这些患者需至少携带一个对Kalydeco敏感的CFTR基因突变。
规格与性状
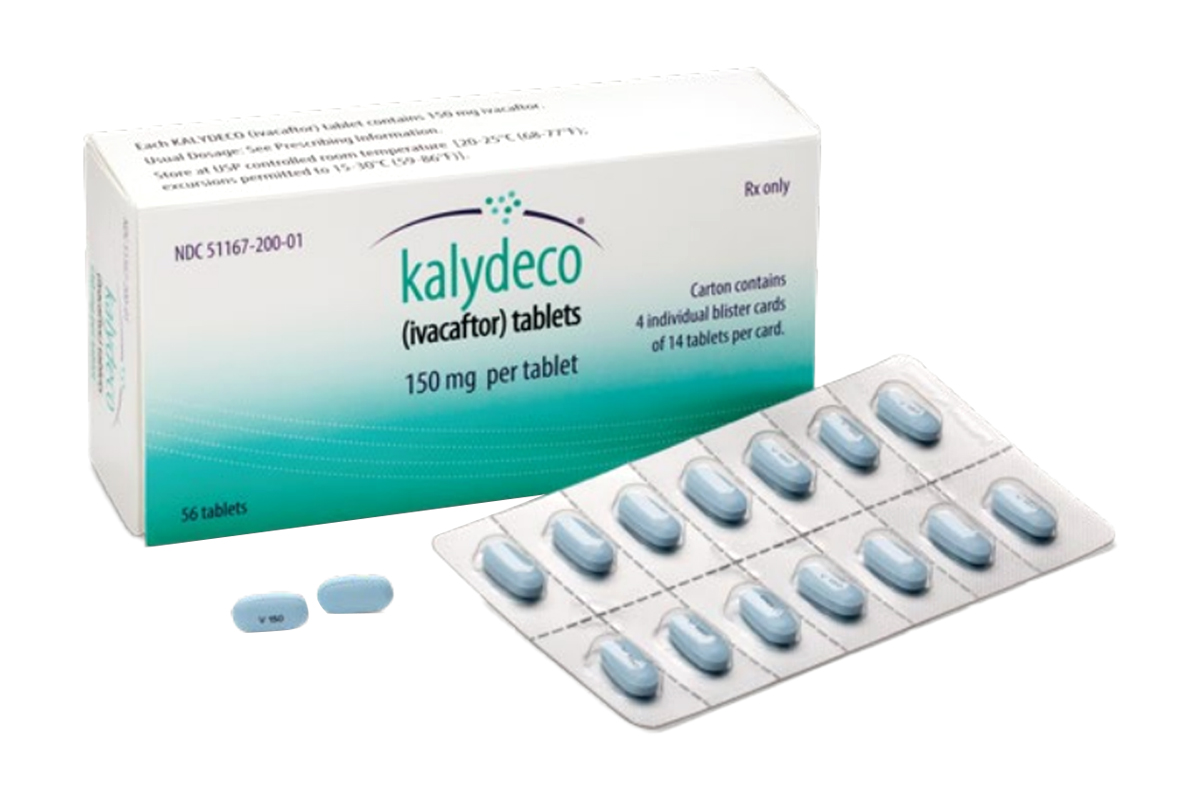
规格:150mg*56片/盒。
性状:为浅蓝色、薄膜包衣。每片片剂一面印有“V150”字样,另一面为空白。
主要成分
活性成分:ivacaftor
辅料:胶体二氧化硅、交联羧甲基纤维素钠、一水乳糖、硬脂酸镁等辅料。
用法用量
1、成人和6岁及以上儿童
每次口服150毫克Kalydeco片剂,每日两次,间隔12小时,随含脂肪的食物一起服用。
2、1个月至6岁以下儿童
根据体重调整Kalydeco口服颗粒剂的剂量,随含脂肪的食物或液体一起服用。
3、漏服处理
若漏服一剂Kalydeco,且距下次服药时间不超过6小时,应尽快补服;
若已超过6小时,则跳过该剂,继续按常规时间服用下一剂,切勿一次服用两剂以弥补漏服的剂量。
不良反应
1、常见不良反应
Kalydeco可能引起的不良反应包括头痛、咽喉痛、上呼吸道感染、鼻塞、腹痛、鼻咽炎、腹泻、皮疹、恶心和眩晕等。
2、严重的不良反应
包括肝酶升高、过敏反应和可能的白内障等。患者在使用Kalydeco期间应定期进行肝功能和眼科检查。
注意事项
1、在使用Kalydeco前,患者应告知医生所有医疗状况,包括肝脏或肾脏问题、过敏史、怀孕或哺乳情况等。
2、Kalydeco可能与其他药物发生相互作用,患者应告知医生当前正在使用的所有药物。
3、避免在服用Kalydeco期间食用含葡萄柚的食物或饮料。
特殊人群用药
对于年龄小于6个月的CF患者,若正在使用中度或强效CYP3A抑制剂,不推荐使用Kalydeco。
对于肝功能损害的患者,可能需要根据病情调整剂量。
禁忌症
尚不明确。
药物相互作用
1、Kalydeco与强效CYP3A诱导剂(如利福平)合用时,可能降低ivacaftor的暴露量,从而降低Kalydeco的疗效。因此,不推荐同时使用。
2、Kalydeco还可能抑制CYP2C9等酶,增加某些药物(如华法林)的暴露量,因此在使用这些药物时需要监测相关指标。
药物过量
Kalydeco过量的处理措施尚不明确。若发生过量,应立即就医。
药代动力学
Kalydeco与含脂肪的食物一起服用时,其暴露量会增加约2.5至4倍。
Kalydeco主要在肝脏代谢,通过粪便排泄。
对于肝功能损害的患者,可能需要调整剂量。
贮存方法
将Kalydeco存储在室温下,即20°C至25°C,远离儿童和宠物。
研发公司
美国Vertex(美国福泰制药)