



仑卡奈单抗(Lecanemab)商品名LEQEMBI,是一种用于治疗阿尔茨海默病的人源化单克隆抗体,可以选择性中和并清除导致阿尔茨海默病神经病变的可溶且有毒性的β-淀粉样蛋白(Aβ)聚集体。那么,仑卡奈单抗(Lecanemab)治疗阿尔茨海默症效果如何?

在阿尔茨海默病患者(证实存在淀粉样蛋白病理学和轻度认知功能障碍的患者 [64%的患者] 或疾病的轻度痴呆阶段 [36%的患者],与3期和4期阿尔茨海默病一致)中开展了一项双盲、安慰剂对照、平行组、剂量探索研究(研究1,NCT01767311),评价了 LEQEMBI 的疗效。研究1有79周的双盲、安慰剂对照期,随后是长达260周的开放标签扩展期,在停止治疗的间隙期(范围9-59个月;平均24个月)后开始。
在研究1中,856例患者随机接受5种剂量之一(其中161例随机接受推荐给药方案10 mg/kg,每两周一次)的 LEQEMBI 或安慰剂 (n = 247)。在随机化的患者总数中,71.4%为ApoEε4携带者,28.6%为ApoEε4非携带者。研究期间对方案进行了修订,不再将ApoEε4携带者随机分配至 10 mg/kg 每两周一次剂量组。接受 LEQEMBI 10 mg/kg 每两周一次治疗6个月或以下的ApoEε4携带者停用研究药物。结果在 LEQEMBI 10 mg/kg 每两周一次组中,30.3%的患者为ApoEε4携带者,69.7%为ApoEε4非携带者。基线时,随机化患者的平均年龄为71岁,范围为50-90岁。50%的患者为男性,90%为白人。
入组患者的临床痴呆评定量表 (CDR) 总分为0.5或1.0,记忆框评分为0.5或更高。所有患者的简易精神状态检查 (MMSE) 评分均≥22,存在情景记忆客观损害,表现为韦氏记忆量表-IV 逻辑记忆II(子量表)(WMS-IV LMII) 中低于年龄校正平均值至少1个标准差。患者入组时伴随或未伴随获批的阿尔茨海默病治疗(胆碱酯酶抑制剂和 N-甲基-D-天冬氨酸拮抗剂美金刚)。
在研究1中,315例患者亚组入组淀粉样蛋白 PET 子研究;其中277例在第79周接受评价。β淀粉样蛋白 PET 子研究的结果见图1和表1。血浆生物标志物见表1。
图1:研究1中的脑淀粉样β斑块减少(淀粉样βPET复合终点、SUVR和 Centiloids 较基线的校正平均变化)
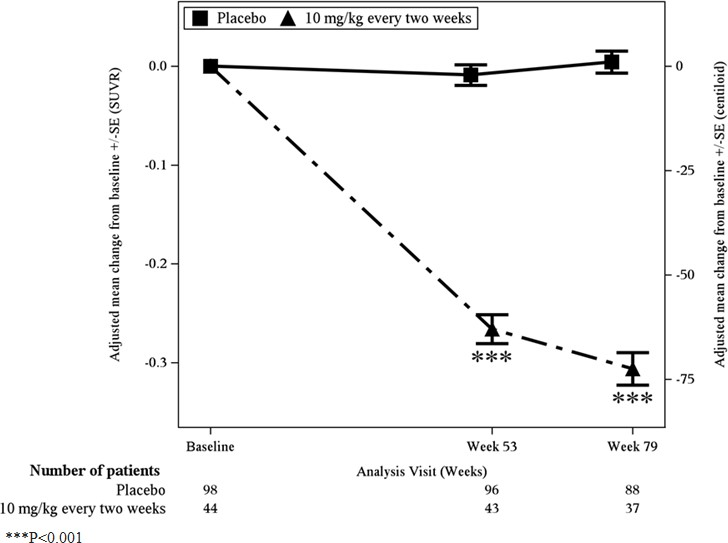
表1:研究1中 LEQEMBI 的生物标志物结果
|
生物标志物终点1 |
LEQEMBI 10 mg/kg,每2周一次 |
安慰剂 |
|
淀粉样βPET复合 SUVR |
N = 44 |
N = 98 |
|
平均基线 |
1.373 |
1.402 |
|
第79周校正后较基线的平均变化较安慰剂的差异 |
-0.306 -0.310(p < 0.001) |
0.004 |
|
β淀粉样蛋白 PET 胶体 |
N = 44 |
N = 98 |
|
平均基线 |
78.0 |
84.8 |
|
第79周校正后较基线的平均变化较安慰剂的差异 |
-72.5 -73.5(p < 0.001) |
1.0 |
|
血浆Aβ42/40 2 |
N = 43 |
N = 88 |
|
平均基线 |
0.0842 |
0.0855 |
|
第79周校正后较基线的平均变化较安慰剂的差异 |
0.0075 0.0054 (p = 0.0036) |
0.0021 |
|
血浆 p-tau181(pg/mL)2 |
N = 84 |
N = 179 |
|
平均基线 |
4.6474 |
4.435 |
|
第79周校正后较基线的平均变化较安慰剂的差异 |
-1.1127 -1.1960(p < 0.0001) |
0.0832 |
主要终点是第53周由CDR-SB、MMSE和 ADAS-Cog 14 的选定项目组成的加权综合评分较基线的变化。第53周时,与安慰剂相比,LEQEMBI在主要终点上减缓进展的可能性为64%或以上,不符合预先规定的80%的成功标准。
关键次要疗效终点包括第79周淀粉样蛋白 PET SUVR 复合终点较基线的变化以及第79周 CDR-SB 和 ADAS-Cog 14 较基线的变化。临床评估结果显示,LEQEMBI组第79周 CDR-SB 和 ADAS-Cog 14 评分较基线的变化小于安慰剂组患者(CDR-SB:-0.40[26%],90%CI[-0.82,0.03];ADAS-Cog 14:-2.31[47%],90%CI[-3.91,-0.72] 。
由此可见,仑卡奈单抗(Lecanemab)治疗阿尔茨海默症效果是十分不错的。
相关热文推荐:仑卡奈单抗(Lecanemab)使用注意事项?
注:文章信息来源于网络,仅供医护人员内部讨论,不作为用药依据,具体用药指引,请咨询主治医师。
