



艾加莫德(Vyvgart Hytrulo)的适应症为重症肌无力。在临床试验中,艾加莫德显示出了一定的疗效。
在对gMG患者进行的双盲、安慰剂对照3期ADAPT试验中,与安慰剂相比,艾加莫德(Vyvgart Hytrulo)显著且快速地降低了疾病负担,并改善了肌肉力量和生活质量。此外,在正在进行的开放标签3期ADAPT+扩展试验的中期分析中,艾加莫德(Vyvgart Hytrulo)为重症肌无力患者提供了一致的具有临床意义的改善。
艾加莫德(Vyvgart Hytrulo)是efgartigimod alfa(一种新生儿 Fc 受体阻滞剂)和透明质酸酶(一种内切糖苷酶)的复方制剂,适用于治疗抗乙酰胆碱受体(AChR)抗体阳性的成人患者的全身性重症肌无力(gMG)。

艾加莫德(Vyvgart Hytrulo)是efgartigimodα和透明质酸酶的复方制剂。Efgartigimod alfa是一种人IgG1抗体片段,可与新生儿Fc受体(FcRn)结合,导致循环IgG减少。透明质酸酶通过解聚透明质酸增加皮下组织的通透性。这种作用是一过性的,皮下组织的通透性在24-48小时内恢复。
对于全身型重症肌无力的有效、靶向、耐受性好、可用于广大患者的治疗方案的需求尚未得到满足。一项研究评估了艾加莫德(Vyvgart Hytrulo)的安全性和有效性,这是一种人IgG1抗体Fc片段,用于降低全身性重症肌无力患者的致病性IgG自身抗体水平。
ADAPT是一项在北美、欧洲和日本15个国家的56个神经肌肉学术和社区中心进行的随机、双盲、安慰剂对照的3期试验。年龄至少为18岁的全身性重症肌无力患者有资格参与本研究,无论抗乙酰胆碱受体抗体状态如何,如果他们的重症肌无力日常生活活动(MG-ADL)评分至少为5分(>50%非眼部),并且正在接受至少一种全身性重症肌无力治疗的稳定剂量。通过交互式反应技术(1:1)将患者随机分配到依夫加替吉莫(10mg/kg)或匹配的安慰剂组,每个周期输注4次(每周1次),根据临床反应在上一周期开始后不超过8周内重复给药。
患者、研究者和临床中心的工作人员都不知道治疗分配。主要终点是在第一个治疗周期中乙酰胆碱受体抗体阳性的MG-ADL应答者(MG-ADL改善持续≥4周≥2分)的比例。主要分析在所有乙酰胆碱受体抗体阳性患者的改良意向治疗人群中进行,这些患者具有有效的基线MG-ADL评估和至少一次基线后MG-ADL评估。安全性分析包括所有随机分配的患者,他们至少接受了一剂或部分剂量的艾加莫德(Vyvgart Hytrulo)或安慰剂。
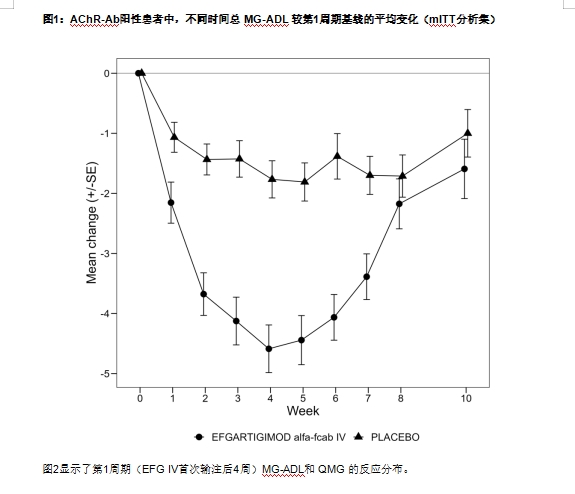
结果:167名患者(84名在艾加莫德组,83名在安慰剂组)被招募,随机分配和治疗。129例(77%)乙酰胆碱受体抗体阳性。在这些患者中,与安慰剂组(64例中的19例[30%])相比,在第1周期中,更多的患者(44例[68%]的艾加莫德组)是MG-ADL反应者,优势比为4.95。
艾加莫德组84名患者中的65名(77%)和安慰剂组83名患者中的70名(84%)出现了治疗中出现的不良事件,最常见的是头痛和鼻咽炎。在安慰剂组中,4名(5%)接受艾加莫德治疗的患者和7名(8%)患者出现了严重的不良事件。每个治疗组中有三名患者(4%)在研究期间停止治疗。没有人死亡。
由此可见,艾加莫德(Vyvgart Hytrulo)对全身型重症肌无力患者具有良好的耐受性和疗效。
艾加莫德(Vyvgart Hytrulo)为皮下注射剂,此外还有静脉注射剂。静脉注射艾加莫德是全球多个国家批准的第一个新生儿Fc受体拮抗剂,包括美国和欧盟,用于治疗抗乙酰胆碱受体(AChR)抗体阳性的成人全身性重症肌无力(gMG),以及日本,用于治疗gMG(无论抗体状态如何)。
总之,使用艾加莫德(Vyvgart Hytrulo)后,患者的病情得到了一定程度的改善,血清IgG水平也得到了降低。同时,艾加莫德还可以提高患者的生活质量,改善其肌肉力量和生活活动能力等方面。有适应症的患者可在咨询医生后用药治疗。
Howard JF Jr, Bril V, Vu T, Karam C, Peric S,
Margania T, Murai H, Bilinska M, Shakarishvili R, Smilowski M,
Guglietta A, Ulrichts P, Vangeneugden T, Utsugisawa K, Verschuuren J,
Mantegazza R; ADAPT Investigator Study Group. Safety, efficacy, and
tolerability of efgartigimod in patients with generalised myasthenia
gravis (ADAPT): a multicentre, randomised, placebo-controlled, phase 3
trial. Lancet Neurol. 2021 Jul;20(7):526-536. doi:
10.1016/S1474-4422(21)00159-9. Erratum in: Lancet Neurol. 2021
Aug;20(8):e5. PMID: 34146511.
注:文章信息来源于网络,仅供医护人员内部讨论,不作为用药依据,具体用药指引,请咨询主治医师。



.png)