Axi-cel(阿基仑赛)是一种自抗体CD19嵌合抗原受体CAR-T细胞疗法,被批准用于治疗≥2线治疗后的复发/难治性大B细胞淋巴瘤(LBCL)患者。
2021年ASH:ZUMA-1研究5年随访数据—Axi-cel(阿基仑赛)治疗难治性大B细胞淋巴瘤患者的关键性研究
ZUMA-1研究是阿基仑赛用于治疗难治性LBCL患者的多中心、单臂、登记性1/2期研究。在ZUMA-1的2年分析中(n=101,自阿基仑赛给药至数据截止中位随访27.1个月),关键性队列1和2的客观缓解率(ORR)为83%(其中58%为完全缓解[CR]),2年总生存率(OS)为50.5%。≥4年随访后(中位随访51.1个月),中位OS为25.5个月,4年OS率为44%。在此,研究人员报告5年随访后ZUMA-1研究2期的最新生存结果,并对12个月和24个月无事件生存(EFS)状态与OS的相关性进行探索性分析。
该研究的主要入选标准:难治性LBCL(DLBCL、PMBCL、tFL);末次化疗无缓解,或ASCT后≤12个月复发;既往应用抗CD20单克隆抗体和蒽环类药物。该研究的主要终点为ORR、输注后第4周进行首次疗效评估。关键次要终点为OS、安全性和转化评估。
研究方法:使用Kaplan-Meier方法评估中位OS、5年生存率和至下次治疗时间。至下次治疗时间定义为,自阿基仑赛输注,至开始新的抗肿瘤治疗的时间,包括CAR-T细胞再次输注,但不包括干细胞移植(SCT),或任何原因导致的死亡。使用经过验证的聚合酶链反应方法(PCR)来检测血液中的CAR-T细胞水平。12个月和24个月EFS和OS相关性的探索性分析。EFS定义为,自阿基仑赛输注至疾病进展、开始新的抗肿瘤治疗(不包括SCT)或任何原因导致的死亡。Kaplan-Meier方法用于评估中位OS、5年OS率、中位EFS、EFS率,以及不同EFS结果与患者的OS比较。
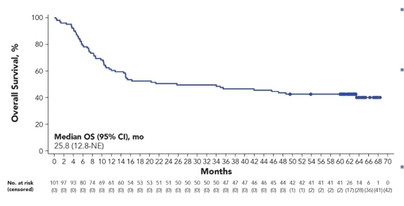
随访5年总生存数据:随访≥5年,阿基仑赛治疗患者的5年OS率为42.6%。完全缓解(CR)患者的5年OS率为64.4%,中位OS未达到;37/59例CR患者在随访5年数据截止时仍生存。自4年数据截止以来,在第63个月观察到1例CR患者死亡,在第54个月观察到1例部分缓解(PR)患者疾病进展。
5年随访中,至下次治疗时间的探索性分析:注射阿基仑赛后,中位至下次抗肿瘤治疗时间为8.7个月,与之前报告相同。5年数据截止时,34例患者仍然生存,且未接受后续治疗(不包括SCT)或阿基仑赛再治疗。与4年数据相比,2例患者因疾病进展接受了新的抗肿瘤治疗。
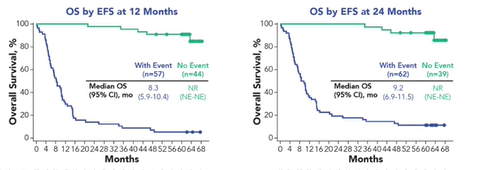
无事件生存EFS的探索性分析:在所有接受治疗的患者中,12个月EFS率为42.8%,24个月EFS率为37.7%。
12个月和24个月EFS分别与OS的相关性分析:在第12个月有EFS(n=57)和无EFS(n=44)事件的患者中,5年OS率分别为5.3%和90.9%。在第24个月有EFS(n=62)和无EFS(n=39)事件的患者中,5年OS率分别为11.3%和92.3%。
研究发现,早期CAR-T细胞扩增峰值与第60个月时的持续缓解有关。第60个月时持续缓解患者的中位CAR-T细胞峰值水平在数值上更高,而在复发和未缓解的患者中则要低很多。根据第0天到第28天曲线下面积评估的CAR-T细胞扩增中也观察到了类似的趋势。
死亡数据分析显示,至数据截止日期,在接受治疗的患者中,58%的患者死亡。在4年数据截止日期之后,1例患者死于继发性恶性肿瘤(LBCL患者CR期间,与既往治疗和/或预处理化疗相关的MDS)。所有患者均未接受免疫球蛋白的静脉输注。5年数据截止时,未报告新的安全性事件,包括无与阿基仑赛相关的严重不良事件,以及无与阿基仑赛相关的继发性恶性肿瘤。
研究结论:
在这项对ZUMA-1研究2期关键性队列的5年更新数据分析中,阿基仑赛使难治性LBCL患者获得长期总生存,且未发现新的安全性事件。在接受治疗的患者中,5年OS率为42.6%;在4年和5年分析之间,至下次治疗时间的曲线保持稳定,92%的患者无需后续治疗仍可生存,提示这些患者可能已被治愈;安全性结果与之前报告中的结果相似,没有观察到新的安全性事件。
持久缓解与CAR-T扩增峰值强烈相关。探索性分析显示,难治性LBCL患者的EFS状态与长期OS呈高度相关性。
这些发现可能支持使用复发难治性LBCL患者1年和2年EFS作为长期OS的替代终点评估。
2021年ASH:ZUMA-1队列6的1年数据—预防性皮质类固醇联合阿基仑赛,用于治疗复发/难治性(R/R)LBCL
ZUMA-1是一项阿基仑赛用于治疗复发/难治性LBCL的登记性1/2期研究。在ZUMA-1关键性队列1+2中,ORR为83%,CR率为58%;中位随访63.1个月,中位OS为25.8个月,5年OS率为43%;≥3级CRS(细胞因子释放综合征)发生率为13%,≥3级NE(甲肾上腺素)发生率为28%。
研究者在持续性地评估CRS和NE的管理,以优化安全性结局。在队列4的安全性管理中,早期应用皮质类固醇和/或托珠单抗似乎可降低≥3级CRS和NE的发生率,且不影响CAR-T细胞的扩增或持续缓解率。队列6评估了在队列4毒性管理方案中加入皮质类固醇的预防性应用,旨在进一步降低CRS和NE的发生率和严重程度。
队列6(n=40)中位随访8.9个月,未观察到≥3级CRS,≥3级NE的发生率较低(13%),缓解率较高(ORR为95%,CR率为80%)。
该研究的主要入选标准:队列1+2,末次化疗无缓解或ASCT后≤12个月复发;队列6,≥2线治疗后的R/R LBCL。
队列6的1年数据分析:截止至2020年12月16日,40例复发/难治性LBCL患者接受阿基仑赛治疗,所有40例患者均可进行有效性和安全性的分析。患者中位年龄为64.5岁,55%的患者ECOG体力状态评分为1,65%患者的疾病分期为III期或IV期,38%的患者已接受≥3次既往治疗。主要终点:CRS和神经系统事件的发生率和严重程度。队列6中无≥3级CRS发生;15%的患者报告≥3级神经系统事件。
先前队列6分析后的安全性数据更新:无新发的CRS病例;2例患者新发4次与阿基仑赛相关神经系统事件:(1)患者1,2级意识状态改变和痫样发作,均发生于第441天(持续时间分别为2天和1天);(2)患者2,1级痴呆(发生于第93天但延迟报道,持续时间277天),5级中毒性脑病发生于第369天(由发生于第351天的4级事件引起)。研究者认为在研究开始之前即存在1例轻度痴呆的病例;5级AE患者因家人拒绝诊断检测和尸检而限制检查,然而磁共振显示脑白质病变,尚未经腰椎穿刺确认。研究者怀疑此结果饿原因为长期免疫抑制导致的机会性感染。2例新发感染,分别发生于第474天的2级肺炎(缓解于第479天,与阿基仑赛无关),和发生于第459天的1级支气管炎(缓解于第459天,与阿基仑赛相关);1例患者因疾病进展死亡。
CAR-T细胞和细胞因子水平的倾向评分比较:在倾向评分匹配前后,2个队列的CAR-T细胞峰值水平相似,队列6中炎症生物标志物峰值(与CAR-T细胞治疗相关的AE有关,包括IFN-y,IL-2,GM-CSF和铁蛋白)均低于队列1+2,支持了临床结果。
研究结果的倾向评分比较:疗效相似。在倾向评分匹配前后,队列6和队列1+2中患者临床疗效保持相似。在安全性方面,在倾向评分匹配前后,与队列1+2相比,队列6中≥3级CRS的发生率较低;在倾向评分匹配前后,与队列1+2相比(中位时间为2天),队列6中至任何级别CRS发作的中位时间有所延迟(中位时间为5天);在倾向评分匹配前后,与队列1+2相比,队列6中至≥3级NE发作饿中位时间似乎延迟(中位时间分别为12天 vs 7天)。
研究结果的倾向评分比较:皮质类固醇和托珠单抗的使用。匹配后,队列1+2的中位皮质类固醇累积剂量是队列6的≈6倍(分别为7418mg和1252mg);尽管匹配后与队列1+2相比,队列6中更多患者需要托珠单抗,但中位托珠单抗累积剂量峰值较低(分别为1000mg和1339mg)。
研究结论:
对ZUMA-1研究队列6进行至少1年的随访,预防性和早期皮质类固醇和/或托珠单抗干预用于毒性管理,继续显示出改善阿基仑赛的获益/风险的潜力,且对药代动力学和/或疗效结果没有负面影响。
尽管受到回顾性和跨队列比较的限制,但研究结果仍得到了与关键队列1+2比较的倾向评分匹配分析的证实。
总体而言,这些发现表明队列6毒性管理策略可以提高阿基仑赛治疗复发/难治性LBCL患者的长期安全性,且不会影响其疗效特征,包括缓解的持久性。
2021年ASH:CIBMTR真实世界研究数据更新—阿基仑赛治疗R/R LBCL:年龄和特定器官功能不全的影响
阿基仑赛是一种自体抗CD19 CAR-T 细胞疗法,美国和欧洲已批准其用于治疗既往≥2线系统性治疗后复发/难治性大B细胞淋巴瘤成人患者。
ZUMA-1研究的5年随访分析(中位随访63.1个月)表明,中位OS为25.8个月,KM估计的5年OS率为43%。
因合并症不符合ZUMA-1入组条件的部分患者可在真实世界中接受阿基仑赛治疗,阿基仑赛真身世界的安全性和有效性结果与ZUMA-1研究基本相似,但符合ZUMA-1入组条件患者的完全缓解率和缓解持续时间更具优势。
研究人员分析了阿基仑赛获批后的安全性研究数据,旨在评估真实世界中年龄和合并症对疗效和安全性的影响。
截至2021年6月22日,共计入组1500例患者,其中1343例患者纳入此项分析。在基线时,682例患者ECOG≥2,和/或伴合并症、和/或伴CNS淋巴瘤/CNS转移,不符合ZUMA-1研究的入组条件。
结果显示,阿基仑赛患者的ORR(客观缓解率)和DOR(缓解持续时间)疗效数据良好。中位DOR尚未达到,预估的1年和2年DOR率分别为64%和57%。中位随访13个月,中位PFS(无进展生存期)为8.8个月,中位OS为22.4个月。
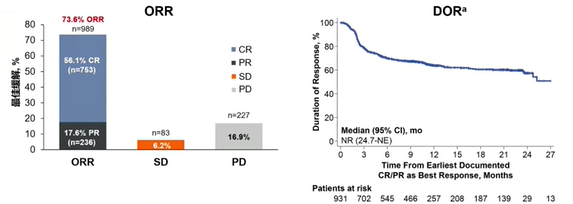
关键因素与疗效结局之间的相关性:
更低的ECOG评分与所有4项疗效指标更好相关;年龄与更差的临床结局无关,高龄患者的ORR疗效反而更好。预先选择的器官功能不全与较差的反应率无相关性;肝脏疾病与更差的DOR、PFS和OS相关,心/脑血管/心瓣膜和肾脏疾病与更差的OS相关。
阿基仑赛的CRS(细胞因子释放综合征)和ICANS发生率与既往报告一致。83%的患者报告CRS,其中≥3级CRS发生率为8%;55%的患者报告ICANS,其中≥3级ICANS发生率为25%。
关键因素与CRS和ICANS之间的相关性:
年龄≥65岁与CRS和ICANS的高风险相关;ECOG评分较高与ICANS的高风险相关;肝脏疾病与≥3级CRS高风险相关。
研究结论:
本研究有效性和安全性终点的结果与ZUMA-1研究及其扩展数据保持一致,验证了使用真实世界的数据来评估上市后CAR-T细胞治疗结果的可行性。
高龄(≥65岁)不影响疗效结局;然而老年患者CRS和ICANS发生率更高。
阿基仑赛患者筛选和治疗决策的过程中,应考虑患者的体力状态。
伴器官功能不全的患者,接受阿基仑赛治疗后一般预后较好,尽管中重度肝脏、肾脏和心脏疾病与更低的总生存期相关。
阿基仑赛可有效治疗复发/难治性大B细胞淋巴瘤,为这类患者带来了新的治疗希望。目前,阿基仑赛在中国的价格已经远低于美国价格,但是我们相信通过与更多的商业保险合作,在联合医保支付方一同探索新的支付模式,将为更多的患者提供阿基仑赛。