



试验显示,帕博利珠单抗(pembrolizumab,Keytruda, 派姆单抗)对于程序性细胞死亡配体-1(PD-L1)阳性的实体瘤患者疗效良好。然而,有关胆道癌(BTC)免疫治疗的数据有限。KEYNOTE-028试验旨在研究PD-L1表达作为BTC免疫治疗生物标志物的预测价值。
在175名患者中,26名胆道癌患者接受了帕博利珠单抗作为二线疗法,并评估了肿瘤反应。根据PD-L1表达将这些患者分为两组(高表达[≥50%]对低表达[<50%]),总缓解率为23%(高PD-L1组56%[5/9]对低PD-L1组6%[1/17],P=0.004)。高PD-L1组的疾病控制率也较高(78%对35%,P=0.019)。
6名应答者在开始使用帕博利珠单抗后显示中位无进展生存期为5.8个月。PD-L1的高表达与帕博利珠单抗的更好反应相关。PD-L1表达可以作为帕博利珠单抗治疗晚期BTC的替代性预测生物标志物。
胆道癌包含一组异质性癌症,包括肝内和肝外胆管癌以及胆囊癌,其临床结果令人沮丧,5年生存率为20-30%。大多数病人在晚期被确诊,姑息性化疗是唯一的选择。

吉西他滨(gemcitabine)联合顺铂(cisplatin)是晚期胆道癌的标准一线疗法,没有标准二线疗法。几种抗PD-1/PD-L1药物在多种实体瘤中显示出长期抗肿瘤作用,目前已被批准用于包括肺癌在内的多种实体癌的标准治疗。
据报道,9.1-72.2%的胆道癌患者有PD-L1表达,因此,抗PD-1或PD-L1药物对于某些胆道癌患者可能是一种有前途的治疗方法。然而,与其他肿瘤相比,胆道癌的免疫治疗数据有限。尽管如此,正在进行的试验(KEYNOTE-028,NCT02054806)的中期结果显示,在PD-L1阳性的晚期胆道癌患者中,帕博利珠单抗(抗PD-1抗体)具有良好的疗效。
临床招募
一项国际临床试验——比较帕博利珠单抗联合化疗对比安慰剂联合化疗一线治疗晚期和/或不可切除的胆道癌的III期试验,正在进行临床招募,具体信息如下:
试验目的:
在患有晚期和/或不可切除的成年胆道癌受试者中,比较帕博利珠单抗+化疗联合方案与生理盐水安慰剂+化疗联合方案作为一线治疗的有效性和安全性
试验设计:
试验分类:安全性和有效性 试验分期:3期 设计类型:平行分组 随机化:随机化 盲法:双盲 试验范围:国际多中心试验
入选标准:
1.组织学确诊为晚期(转移性)和/或不可切除的(局部晚期)胆道癌(肝内或肝外胆管癌或胆囊癌)。 2.有由当地研究中心研究者评价的符合基于RECIST1.1的可测量疾病。 3.具有HBV/HCV感染病史的受试者只要满足方案要求即有资格参加本研究。 4.男性或女性,在签署知情同意书时至少年满18岁(含)。 5.预期寿命3个月以上。 6.可提供存档肿瘤组织样本或新鲜获得的空芯针或切除活检肿瘤组织样本。 7.充分的器官功能。
排除标准:
1.既往接受过晚期(转移性)或不可切除的(局部晚期)胆道癌(肝内或肝外胆管癌或胆囊癌)的系统性治疗,允许的辅助治疗除外。辅助治疗应在确诊晚期和/或不可切除疾病前至少6个月完成。 2.患有壶腹部癌。 3.患有小细胞癌、神经内分泌肿瘤、淋巴瘤、肉瘤和/或粘液性囊性肿瘤。 4.既往接受过抗PD-1、抗-PD-L1或抗PD-L2药物的治疗或针对另一种刺激性或共抑制性T细胞受体的药物(例如CTLA-4、 OX-40、CD137)的治疗。 5.根据当地研究中心研究者的评估,有中枢神经系统(CNS)转移和/或癌性脑膜炎的已知病史或任何证据。 6.接受过同种异体组织/实体器官移植的受试者。 (注:最终入选由研究人员确定)
主要研究中心所在地(具体启动情况以后期咨询为准)
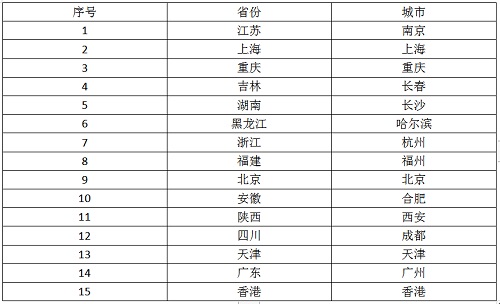
如果想了解更多信息,可联系医伴旅团队,我们将为您解惑。联系电话:400-001-2811
参考文献: 论文:High PD‑L1 expression is associated with therapeutic response to pembrolizumab in patients with advanced biliary tract cancer
注:文章信息来源于网络,仅供医护人员内部讨论,不作为用药依据,具体用药指引,请咨询主治医师。
