



导语:抗体-药物偶联物(ADC)的发展为乳腺癌患者打开了新的治疗大门,为各种类型的乳腺癌患者提供了治疗新选择。
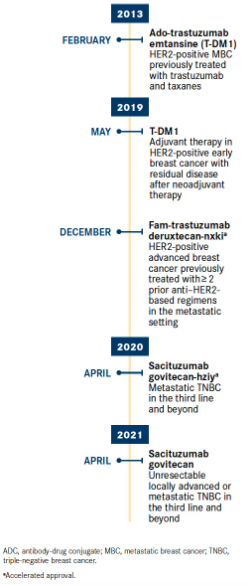
2013年,ado-trastuzumab emtansine (T-DM1;Kadcyla;恩美曲妥珠单抗)获得FDA批准用于治疗HER2阳性转移性乳腺癌(MBC)患者,成为首个可用于实体瘤的抗体-药物偶联物(ADC)。从那时起,ADC就成为肿瘤药物治疗中发展最快的一类。在乳腺癌中,ADC随着适应症、靶点和药物设计的进步而不断发展。
(来源:onclive.com)
该领域的最新进展包括:sacituzumab govitecan-hziy (Trodelvy,戈沙妥组单抗)获得了FDA的全面批准,这是一种首创的Trop-2靶向ADC,用于治疗转移性三阴性乳腺癌(TNBC)患者。与此同时,根据DESTINY-Breast03试验(NCT03529110)的顶线数据,fam-trastuzumab deruxtecan-nxki[ (Enhertu,曲妥珠单抗重组冻干粉注射剂);最初于2019年获批的HER2靶向ADC]在既往接受过治疗的HER2阳性MBC患者中的疗效要优于T-DM1。
目前,越来越多的ADC正在研发用于治疗乳腺癌,它们具有多种新颖的设计,包括一些处于后期临床试验阶段的药物。如果这些药物的治疗效果与它们在早期试验中的一致,那么ADC似乎将在未来几年进一步塑造乳腺癌的治疗格局。
治疗乳腺癌领域的成功之路
ADC有时被称为癌症治疗设备中的“特洛伊木马”,它已经发展了几十年,最初用于治疗血液系统恶性肿瘤。这些药物由3个主要成分组成:靶向肿瘤相关抗原的单克隆抗体(mAb)、细胞毒性药物(有效载荷)和连接它们的连接物。
T-DM1由靶向HER2的单克隆抗体 trastuzumab通过不可降解的连接物结合到emtansine(一种有效的微管蛋白聚合抑制剂)上。T-DM1的药物抗体比(DAR)为3.5,这意味着trastuzumab的每个分子平均携带3.5个emtansine分子。
基于3期EMILIA试验(NCT00829166)的结果,T-DM1最初获批用于治疗HER2阳性MBC患者。与Lapatinib[(Tykerb,拉帕替尼);一种HER2/EGFR抑制剂]加capecitabine [(Xeloda,卡培他滨);通过减少胸腺嘧啶核苷来抑制DNA合成]联合疗法相比,T-DM1显著改善了患者的中位无进展生存期(PFS)和总生存期(OS)。T-DM1组和拉帕替尼/卡培他滨组的中位无进展生存期分别为9.6个月和6.4个月;中位总生存期分别为30.9个月和25.1个月。
在前线治疗环境中,MARIANNE试验(NCT01120184)证明T-DM1无论是单药疗法或联合pertuzumab [(Perjeta,帕妥珠单抗);一种HER2靶向单克隆抗体]在治疗HER2阳性MBC方面的效果并不差于trastuzumab (Herceptin,赫赛汀)加紫杉烷。非劣效性基于中位PFS数据,其中T-DM1单药治疗为14.1个月、T-DM1 +帕妥珠单抗为15.2个月、赫赛汀+紫杉烷为13.7个月。虽然优越性尚未确定,但新组合方案通常毒性较小,而且能够为患者提供更好的生活质量。
根据国家综合癌症网络指南,尽管帕妥珠单抗、赫赛汀和紫杉烷的组合方案为HER2阳性MBC患者的首选方案,但T-DM1为不适合紫杉烷治疗的患者提供了一种新治疗选择。
2019年,基于KATHERINE试验(NCT01772472)的结果,T-DM1获批用于HER2阳性早期乳腺癌患者的辅助治疗;在接受过赫赛汀和紫杉烷辅助治疗后有残留侵袭性疾病的患者中,与赫赛汀相比,T-DM1将无侵袭性疾病的生存率提高了50%。
可用的治疗选择日渐增多
研究人员正致力于创造更有效、毒性更低的ADC。曲妥珠单抗重组冻干粉注射剂由人源化免疫球蛋白G1 HER2靶向单克隆抗体组成,其序列与赫赛汀相同,trastuzumab通过溶酶体组织蛋白酶选择性切割的连接物与拓扑异构酶I抑制剂deruxtecan 结合。
每个抗体分子平均有8个deruxtecan分子,曲妥珠单抗重组冻干粉注射剂的DAR要高于T-DM1。历史上,增加药物的DAR会对其药代动力学产生负面影响,但曲妥珠单抗重组冻干粉注射剂并非如此,因为它具有新颖的连接设计。该药物中deruxtecan的有效载荷也比T-DM1具有更强的膜渗透性。
基于2期DESTINY-Breast01研究(NCT03248492),2019年12月曲妥珠单抗重组冻干粉注射剂于得加速批准,用于治疗HER2阳性MBC患者,这些患者在转移环境中接受过至少两次HER2靶向治疗。该新型药物诱导的客观缓解率(ORR)为60.9%,中位缓解持续时间(DOR)为14.8个月。
许多评估曲妥珠单抗重组冻干粉注射剂的临床试验正在进行中,包括在DESTINY-Breast03研究中与T-DM1进行头对头比较。初步分析的结果首次在2021年欧洲医学肿瘤学会大会上公布。数据截止时,在随机分组的524例患者中,与T-DM1相比,曲妥珠单抗重组冻干粉注射剂显著改善了中位无进展生存期。尽管曲妥珠单抗重组冻干粉注射剂组12个月的总生存率在数值上较高(94.1% vs 85.9%),但并没有统计学显著性。
在2021年圣安东尼奥乳腺癌研讨会(2021年SABCS)上发表的DESTINY-Breast03研究的探索性分析结果显示,曲妥珠单抗重组冻干粉注射剂在多个亚组(包括基线脑转移患者[n= 82])中观察到一致的中位无进展生存期获益,曲妥珠单抗重组冻干粉注射剂组为15个月,T-DM1组为3个月。
其他几个HER2靶向ADC正在临床开发中,包括vic-trastuzumab duocarmazine(SYD985),其中一个可切割的连接物将trastuzumab与DNA烷基化剂的前药duocarmycin-hydroxybenzamide-azaindole连接。
尽管其DAR(2.8)低于T-DM1(3.5),但SYD985在临床前模型中显示出更高的抗肿瘤活性。在3期TULIP试验(NCT03262935)中,比较了SYD985和医生选择的方案治疗HER2阳性MBC患者(接受过治疗)的疗效。SYD985显著改善了中位无进展生存期。SYD985组最常见的不良反应(AEs)是结膜炎、角膜炎和疲劳。
其他值得注意的HER2靶向ADC包括:ARX788,它具有微管蛋白抑制剂有效载荷;ZW49是一种双特异性ADC,采用同时靶向HER2上的trastuzumab- 和pertuzumab-结合位点的抗体;以及BDC-1001,它使用Toll样受体激动剂作为有效载荷,旨在刺激抗肿瘤免疫反应,而不是直接杀死肿瘤细胞。相关开发公司表示,ZW49和BDC-1001在正在进行的1/2期临床试验中也显示出有希望的初步活性。
ARX788在2021年SABCS的演示中被重点介绍,在ACE-Breast-01研究(CTR20171162)中,对重度预处理的HER2阳性MBC患者进行了研究,29例患者每三周接受ARX788 1.5 mg/kg,客观缓解率(ORR)为66%,中位缓解持续时间为14.4个月,疾病控制率(DCR)为100%。值得注意的是,在之前接受过HER2靶向ADC治疗的5例患者中产生的ORR为80%。ARX788耐受性良好,大多不良反应为1或2级。FDA已授予ARX788快速通道指定,用于治疗重度预处理的HER2阳性MBC患者。
(来源:onclive.com)
治疗不局限于HER2
据估计,15%至20%的乳腺癌被归类为HER2阳性,HER2蛋白表达水平较高,定义为免疫组织化学(IHC)评分3+,和/或通过原位杂交HER2基因扩增。高达50%的患者被归类为HER2低表达(IHC1+或2+,无基因扩增)。
在治疗决策方面,HER2低表达的乳腺癌目前被归为HER2阴性乳腺癌,因此不适合进行HER2靶向治疗。然而,这种情况可能会改变,因为具有更高杀伤力的新型ADC可能在这一患者群体中具有临床活性。
曲妥珠单抗重组冻干粉注射剂组和SYD985都正在HER2低表达的乳腺癌患者的临床试验中进行评估,初步数据正在形成。在一项1b期试验(NCT02564900)中,评估了曲妥珠单抗重组冻干粉注射剂组在实体瘤中的作用,54例重度预处理的晚期HER2低表达乳腺癌患者接受的剂量为5.4或6.4 mg/kg。结果显示,ORR为37.0%,中位DOR为10.4个月。
两项3期临床试验正在进行中,比较了曲妥珠单抗重组冻干粉注射剂和研究者选择的化疗方案治疗HER2低表达MBC患者的疗效。在招募已经完成的DESTINY-Breast04试验(NCT03734029)中,患者之前接受过1或2次化疗(激素受体可能呈阳性或阴性),而在DESTINY-Breast06试验(NCT04494425)中,患者至少接受过2次内分泌治疗,且激素受体呈阳性。
在转移性实体瘤患者中进行的SYD985首次人体研究(NCT02277717)招募了95例在剂量扩展队列中可评估的MBC患者的。结果显示,HER2阳性队列(n = 48)的ORR为33%;HER2低表达且激素受体阳性队列(n = 32)的ORR为28%;HER2低表达且激素受体阴性队列(n = 15)的ORR为40%。所有缓解均为部分缓解(PRs)。
TNBC的Trop-2表达及其他突变的治疗
TNBCs不表达HER2,因此,替代性抗原靶点正在研究中。对Trop-2(一种乳腺癌中过度表达的跨膜糖蛋白)的研究已经开发了戈沙妥组单抗(Sacituzumab govitecan)。
戈沙妥组单抗是一种首创的Trop-2靶向ADC,其中一个Trop-2单克隆抗体通过可切割的连接物与拓扑异构酶I抑制剂SN-38结合。戈沙妥组单抗具有较高的DAR(7.6),并在临床前研究中显示出强大的杀伤力。
2020年4月,FDA加速批准戈沙妥组单抗用于治疗TNBC患者(在转移环境中至少接受过2种治疗方案)。这一决定是基于1/2期IMMU-132-01研究(NCT01631552)的结果,该研究招募了108例既往治疗过的转移性TNBC患者。ORR为33.3%,中位DOR为7.7个月,治疗耐受性良好。
一年后,基于验证性3期ASCENT试验(NCT02574455)的结果,戈沙妥组单抗获得FDA的完全批准。结果显示,与化疗相比,戈沙妥组单抗可以显著延长晚期转移性TNBC患者(既往接受过至少两次标准化疗方案,包括1次紫杉烷)的中位PFS和中位OS。
高Trop-2表达在多种乳腺癌亚型中常见,IMMU132-01研究招募了一组54例接受戈沙妥组单抗治疗的激素受体阳性/HER2阴性MBC患者。ORR为31.5%,中位DOR为8.7个月。在3期TROPiCS-02 研究(NCT03901339)中,正在比较戈沙妥组单抗和化疗治疗这种乳腺癌亚型的疗效。
第二种Trop-2靶向ADC, datopotamab deruxtecan,也正处于临床开发中。正在进行的1期TROPION-PanTumor01试验(NCT03401385)的转移性TNBC队列的结果在2021年的SABCS上公布,其中大多数受试者已经接受了2种或以上的治疗[包括戈沙妥组单抗(16%)]。在38例可评估反应的患者中,ORR为39%,均为部分缓解,疾病控制率为84%。不良反应包括恶心、口腔炎、脱发、呕吐和疲劳。
替代性靶点的治疗
HER酪氨酸激酶受体家族的另一个成员HER3能够促进HER2的致癌活性。HER3在乳腺癌中过度表达,与预后不良以及对HER2靶向治疗和内分泌治疗的耐药性有关。
Patritumab deruxtecan (HER3-DXd)是一种HER3靶向ADC,由单克隆抗体Patritumab通过一种新的可切割连接物与deruxtecan结合而成,该连接物允许在不损害药物理化特性的情况下获得高DAR (8)。
在一项正在进行的1/2期研究(NCT02980341)中,HER3-DXd在重度预处理的激素受体阳性、HER2阴性MBC患者(无论HER3表达是高还是低)中显示出有希望的抗肿瘤活性,并且具有良好的耐受性。
同时,一项机会窗研究TOT-HER3(NCT04610528)的中期分析数据显示,单剂量HER3-DXd (6.4 mg/kg)与初治的激素受体阳性、HER2阴性、可手术的原发性乳腺癌患者的临床反应有关。
目前,正在探索ADC治疗乳腺癌中的其他几个抗原靶点,其中包括LIV-1蛋白和叶酸受体-α(这两种蛋白在乳腺癌中都高度表达)。靶向LIV-1蛋白的Ladiratuzumab vedotin和靶向叶酸受体-α的MORAb-202均处于临床开发的早期阶段。
抗体-药物偶联物(ADC)的快速发展有望改变乳腺癌患者的治疗格局,为患者带来更快、更有效的治疗方法。
参考资料:
https://www.onclive.com/view/next-generation-antibody-drug-conjugates-make-their-mark-in-breast-cancer
注:文章信息来源于网络,仅供医护人员内部讨论,不作为用药依据,具体用药指引,请咨询主治医师。
