



瑞武丽珠单抗(Ravulizumab)适用于治疗一个月及以上患有
阵发性睡眠性血红蛋白尿症(PNH)的成人及儿童患者。
瑞武丽珠单抗(Ravulizumab)适用于治疗一个月及以上环保油非典型溶血性尿毒症综合征(aHUS)的成人及儿童患者,以抑制补体介导的血栓性微血管病(TMA)。
使用限制:不适用于治疗与志贺毒素大肠杆菌相关溶血性尿毒症综合征(STEC-HUS)的患者。
瑞武丽珠单抗(Ravulizumab)适用于抗乙酷胆碱受体(AChR)抗体阳性的全身性重症肌无力(gMG)成年患者的治疗。
瑞武丽珠单抗(Ravulizumab)已在中国香港、中国台湾上市,但截至目前2023年12月8号,还没有在中国大陆上市。
此外,瑞武丽珠单抗(Ravulizumab)还在美国、加拿大、法国、日本、德国、韩国等国家上市。
一个月及以上的成人或儿童患者可使用瑞武丽珠单抗(Ravulizumab)进行静脉输注(用于静脉给药的Ravulizumab小瓶),或在成人患者中使用用于维持的皮下注射(用于皮下给药的Ravulizumab体内给药系统)。小瓶仅用于静脉注射,而体内给药系统(预填充药筒和体内注射器)仅用于皮下维持。
根据现行ACIP指南为患者接种脑膜炎球菌疾病疫苗,以降低严重感染的风险。如果必须立即开始瑞武丽珠单抗(Ravulizumab),并且在开始瑞武丽珠单抗(Ravulizumab)治疗前不到2周接种疫苗,则为患者提供2周的抗菌药物预防。
成人和儿童PNH、aHUS或gMG患者的静脉给药对于体重大于或等于 5 kg、患有 PNH或aHUS 的一个月大或以上的成人和儿童患者,或体重大于或等于40 kg的gMG 成人患者,推荐的静脉注射瑞武丽珠单抗(Ravulizumab)负荷和维持剂量基于患者的体重,持剂量每4或8周给药一次,从负荷剂量后2周开始。
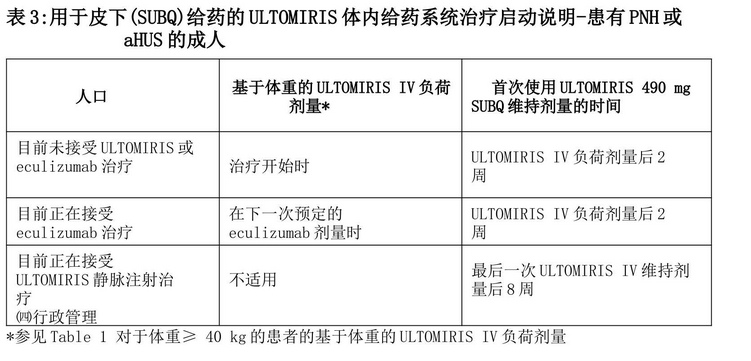
瑞武丽珠单抗(Ravulizumab)的皮下(SUBQ)给药不被批准用于儿科患者对于体重大于或等于40 kg的PNH或aHUS成年患者,推荐的皮下瑞武丽珠单抗(Ravulizumab)维持剂量为490mg,每周一次。
490mg剂量的瑞武丽珠单抗(Ravulizumab)通过2个体内给药系统给药。每个体内给药系统由1个体内注射器和1个含有245mg ravulizumab的预装药筒组成。皮下给药方案允许偶尔在预定给药日的1天内变化,但后续剂量应根据原方案给药。
使用无菌技术制备瑞武丽珠单抗(Ravulizumab),如下所示:
1、待稀释的小瓶数量根据单个患者的体重和处方剂量确定。
2、稀释前,目视检查小瓶中的溶液:溶液应不含任何颗粒物质或沉淀。如果有颗粒物质或沉淀的证据,不要使用。
3、从适当数量的小瓶中抽取计算体积的瑞武丽珠单抗(Ravulizumab),并在输液袋中使用0.9%3.氯化钠注射液(美国药典)稀释至最终浓度。
4、如果稀释的瑞武丽珠单抗(Ravulizumab)输注液没有立即使用,考虑到预期的输注时间,在52°C-8°C(36°F-46°F)下冷藏储存不得超过24小时。从冰箱中取出后,如果用30mL的瑞武丽珠单抗(Ravulizumab)样品瓶配制,应在6小时内注射稀释的ULTOMIRIS输注液。如果用3mL或1 mL的瑞武丽珠单抗(Ravulizumab)样品瓶配制,应在4小时内注射。
5、给药前,将混合物调节至室温(18°C-25°C,64°F-77°F)。不要用微波炉或除环境空气温度以外的任何热源加热混合物。只要溶液和容器允许,注射用药品在给药前应目视检查是否有颗粒物质和变色。
瑞武丽珠单抗(Ravulizumab)是一种末端补体抑制剂,以高亲和力特异性结合补体蛋白C5,从而抑制其裂解为C5a(促炎过敏毒素)和C5b(膜攻击复合物[MAC或C5b-9]的起始亚单位),从而防止MAC 形成。
瑞武丽珠单抗(Ravulizumab)抑制 PNH 患者补体介导的血管内溶血,抑制aHUS 患者补体介导的血栓性微血管病(TMA)。
瑞武丽珠单抗(Ravulizumab)在gMG 患者中发挥其治疗作用的确切机制尚不清楚,但推测涉及减少神经肌肉接头处的末端补体复合物C5b-9 沉积。
瑞武丽珠单抗(Ravulizumab)禁用于以下人群:
1、患有未确诊脑膜炎奈瑟球菌感染的患者。
2、目前未接种脑膜炎奈瑟菌疫苗的患者,除非延迟瑞武丽珠单抗(Ravulizumab)治疗的风险大于发生脑膜炎球菌感染的风险。
1、PNH患者最常见的不良反应为上呼吸道感染和头痛。皮下注瑞武丽珠单抗(Ravulizumab)的患者最常见不良反应为注射部位反应和腹泻。
2、aHUS 患者最常见的不良反应为腹泻、恶心、上呼吸道感染、呕吐、头痛、高血压和发热。
3、gMG 成年患者最常见的不良反应为腹泻和上呼吸道感染。
1、发热:使用瑞武丽珠单抗(Ravulizumab)发热的患者可通过物理方法降温,例如额头贴退热贴,或者温水擦拭身体,若体温较高可使用布洛芬等退热药物治疗。
2、高血压:高血压的患者在治疗期间应定期监测血压,并低盐饮食,必要时使用降压药控制血压。
3、腹泻:腹泻患者应注意腹部的保暖,避免腹部受凉刺激胃肠道蠕动导致腹泻加重,同时避免进食凉性食物。
4、恶心、呕吐:建议患者注意饮食,避免进食油条、炸串、炸鸡等油腻性食物,以免加重恶心症状,也可遵医嘱使用治疗止吐药治疗。
5、头痛:头痛患者应注意情绪的波动,避免情绪激动,治疗期间注意休息,保证充足睡眠,以免休息不好导致头痛加重。
6、输液相关反应:出现输液相关反应的患者可在医生的指导下对症治疗,例如发生过敏反应,应立即停止输液,并采取抗过敏治疗,同时需要密切观察患者的病情变化,并根据需要进行进一步的治疗。
此外,治疗期间患者还可能出现感染等其他不良反应,建议密切观察自身反应,出现不适后及时治疗。
CHAMPION-NMOSD (NCT04201262)是一项3期、开放标记、外部对照的干预性研究,用于评估末端补体抑制剂瑞武丽珠单抗(Ravulizumab)在抗水通道蛋白4抗体阳性(AQP4+)视神经脊髓炎谱系障碍(NMOSD)成年患者中的疗效和安全性。、瑞武丽珠单抗(Ravulizumab)与批准的治疗性eculizumab结合相同的补体成分5表位,但具有更长的半衰期,从而延长了给药间隔(8周对2周)。
eculizumab的可用性排除了CHAMPION-NMOSD中同时使用安慰剂对照的可能性;因此,eculizumab期试验预防的安慰剂组(n= 47)被用作外部对照。患者在第1天接受基于体重的静脉注射瑞武丽珠单抗(Ravulizumab),在第15天接受维持剂量,然后每8周一次。主要终点是首次判定试验复发的时间。
结果:达到了主要终点,服用瑞武丽珠单抗(Ravulizumab)的患者(n = 58)没有判定复发(在84.0患者年的治疗期间),而安慰剂预防组有20名患者判定复发。瑞武丽珠单抗(Ravulizumab)的中位(范围)研究期随访时间为73.5 周。大多数治疗中出现的不良事件为轻度/中度,没有死亡报告。
解释:瑞武丽珠单抗(Ravulizumab)显著降低AQP4+ NMOSD患者的复发风险,在所有批准的适应症中,其安全性与eculizumab和Ravulizumab一致。
瑞武丽珠单抗Ultomiris(Ravulizumab)港版300mg一盒的参考价约为70150元。
注:文章信息来源于网络,仅供医护人员内部讨论,不作为用药依据,具体用药指引,请咨询主治医师。

.png)
.png)
.png)