



《柳叶刀》上公布的数据显示,在HER2阳性早期乳腺癌患者的新辅助治疗中,根据第7周期的帕妥珠单抗血清谷浓度,皮下注射帕妥珠单抗(pertuzumab,Perjeta)和曲妥珠单抗(trastuzumab,Herceptin)联合hyaluronidase-zzxf(Phesgo),与静脉输注帕妥珠单抗+曲妥珠单抗相比,具有非劣性。
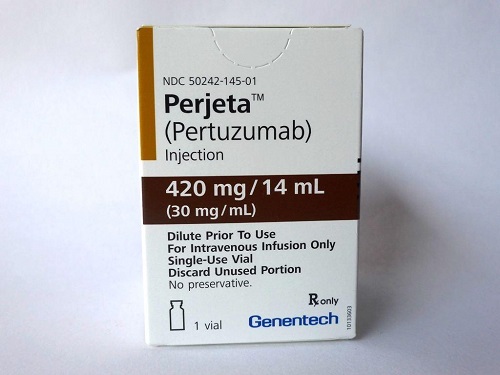
概述
3期FeDeriCa试验(NCT03493854)的数据达到了其主要终点,与静脉输注配方相比,展示出可比的总病理完全缓解率,同时也产生了相似的安全性。与其他研究帕妥珠单抗、曲妥珠单抗和化疗用于治疗HER2阳性早期乳腺癌患者的试验相比,这些数据也具有优势,进一步支持了FDA对该药的批准。
由Antoinette R. Tan博士领导的研究人员写道:“总的来说,本试验的固定剂量组合+化疗的疗效和安全性数据与已知的帕妥珠单抗+曲妥珠单抗+化疗治疗HER2阳性乳腺癌的疗效和安全性相一致。”
试验发现
2018年6月14日至12月24日,患者被随机分为2组,其中252名患者接受静脉输注,248名患者接受固定剂量组合。
研究人员测量了皮下给药vs静脉给药的帕妥珠单抗血清谷浓度的几何平均比,比值为1.22(90%CI,1.14-1.31)。
常见的3/4级不良事件(AE)包括中性粒细胞减少(静脉输注组为13%,固定剂量组为14%)、中性粒细胞计数下降(12%对11%)、发热性中性粒细胞减少(6%对6%)、腹泻(5%对7%)和白细胞计数下降(7%对4%)。
两组均有10%的患者出现治疗相关严重不良事件,每组有1例不良事件导致的死亡,但均与HER2靶向治疗无关。
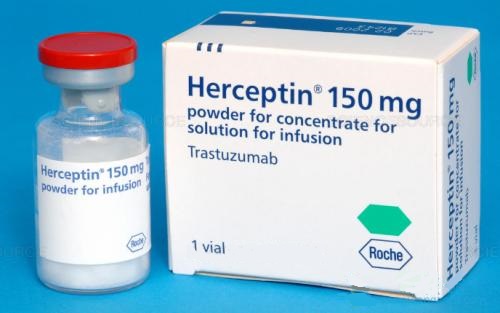
结果分析
研究人员写道:“该试验结果证实了皮下注射帕妥珠单抗+曲妥珠单抗的固定剂量组合在新辅助治疗中,提供了不逊于静脉输注帕妥珠单抗+曲妥珠单抗的血清谷浓度,并且具有可比的总病理完全缓解率和可比的安全性,该结果增加了目前对肿瘤中单克隆抗体皮下给药的了解。”
该试验的安全人群包括至少接受过1剂研究药物的患者,包括化疗或HER2靶向治疗。虽然招募、新辅助治疗和手术都已完成,但辅助治疗和随访目前仍在进行中。
研究人员表示,安全性、有效性和药代动力学结果尚不可用,因为标准治疗要求HER2靶向治疗持续18个周期。研究小组期望固定剂量组合的长期安全性和有效性数据与静脉输注的安全性和有效性相似。
研究人员总结说:“总的来说,证据表明,相比静脉输注,皮下注射单克隆抗体可以更快、更方便、微创地治疗HER2阳性乳腺癌。”
注:文章信息来源于网络,仅供医护人员内部讨论,不作为用药依据,具体用药指引,请咨询主治医师。
