



一项针对2期DREAMM-2试验的分析显示,单药belantamab mafodotin-blmf对接受过至少三种治疗的复发或难治性多发性骨髓瘤患者有效且可耐受。

疗效和安全性不受既往治疗次数的影响。因此,Belantamab mafodotin对于复发或难治性骨髓瘤是一种有效的治疗选择,包括先前治疗负担高且预后较差的患者。
DREAMM-2试验
2期DREAMM-2临床试验是一项正在进行的开放标签研究,检测单药belantamab mafodotin治疗之前至少接受过3种治疗,且对免疫调节药物或蛋白酶体抑制有耐药性患者的疗效,每3周2.5或3.4 mg/kg。
此前的一项分析发现,belantamab mafodotin作为单一药物具有深入持久的临床活性和可控的安全性。在ASH会议上提出的事后分析,根据研究开始前接受治疗的患者数量,研究了belantamab mafodotin(每3周2.5 mg/kg)的安全性和有效性。106例患者被分为两个亚群:之前接受过3 - 6种治疗的患者和之前接受过7种或更多治疗的患者。主要终点为客观缓解率。
安全性分析的重点是关于角膜的不良事件,由眼科护理专业人员进行定期眼科检查确定。
患者在人口统计学和疾病特征方面匹配良好。每个预处理组的所有患者对免疫调节药物、蛋白酶体抑制剂和抗CD38抗体daratumumab(达雷木单抗)均不耐受(即三难治性)。
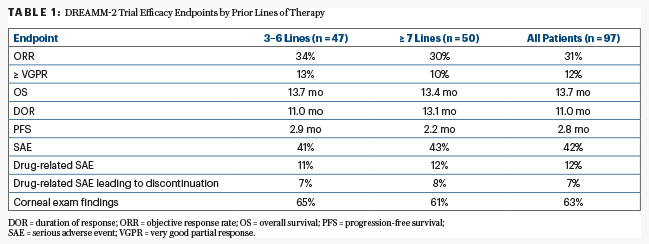
表1显示了两个预处理亚组的疗效终点,显示了每个队列的总生存期超过13个月,且缓解持久。Lonial博士报告说,预处理程度较低的患者无进展生存率略高。
安全性:
belantamab mafodotin的安全性在两个队列中是相似的,不良事件、严重不良事件、剂量调整的发生率相似,停药率相对较低。
注:文章信息来源于网络,仅供医护人员内部讨论,不作为用药依据,具体用药指引,请咨询主治医师。
