



不管是靶向治疗还是免疫治疗,都给晚期肝癌患者带来了希望。面对靶向治疗带来的瓶颈,免疫治疗赋予了新期望。免疫治疗与以往传统治疗不同,它并不直接作用于肿瘤细胞本身,而是通过解除对免疫细胞的抑制,激活患者自身的免疫系统来抗击肿瘤,从而达到杀灭肿瘤的目的。
PD-1程序性死亡受体1,是一种重要的免疫抑制分子。以PD-1为靶点的免疫调节对抗肿瘤、抗感染、抗自身免疫性疾病及器官移植存活等均有重要意义。纳武单抗(nivolumab)是首个获批用于肝癌的单克隆PD-1抗体,在接受过索拉非尼治疗的患者中,中位总生存期可达15.6个月。另一款人源化单克隆PD-1抗体帕博利珠单抗(pembrolizumab)治疗肝癌患者,疾病控制率为61.5%,12个月的总生存率为53.6%。

随着相关研究的进展,肝癌免疫治疗迅速进入新时代。当前,结构独特的PD-1抗体替雷利珠单抗(BGB-A317)倍受期待。替雷利珠单抗注射液,是一款人源化IgG4抗PD-1单克隆抗体,2019年国家药品监督管理局(NMPA)批准上市。在肝癌的临床研究中,替雷利珠单抗的疗效和安全性也已得到了初步的验证,I/II期研究数据显示:替雷利珠单抗单药治疗不可手术晚期肝细胞癌患者的客观缓解率(ORR)为17%,安全性良好,3级及以上不良反应发生率较低。
医伴旅了解到目前正在开展替雷利珠单抗联合仑伐替尼在晚期肝癌一线治疗的研究,符合临床项目报名标准的患者可以踊跃报名,我们将为大家提供最适合的临床项目。
试验药物:
BGB-A317注射液
适应症:
肝细胞癌
临床试验信息:
试验分类:安全性和有效性 试验目的:主要目的 评估总缓解率(ORR)(研究中心影像学评估机构根据RECIST1.1标准) 2. 次要目的 评估安全性和耐受性 评估总缓解率(ORR)(研究者根据RECIST v1.1标准) 评估总缓解率(ORR)(研究者和研究中心影像学评估机构分别根据mRECIST和 iRECIST标准) 评估缓解持续时间(DOR)、疾病控制率(DCR)、无进展生存期(PFS)(研究者和研究中心影像学评估机构分别根据RECIST v1.1和 iRECIST标准)
试验分期:II期 设计类型:单臂试验 随机化:非随机化 盲法:开放 试验范围:国内试验 年龄:18岁(最小年龄)至 70岁(最大年龄) 性别:男+女 健康受试者:无
主要入选标准:
1.签署ICF当天年龄 ≥ 18岁且 ≤ 70岁 2.不可切除的局部晚期或者转移性HCC,并且必须经组织学或细胞学确认 3.巴塞罗那临床肝癌分期(BCLC)C期疾病或BCLC B期疾病,不适合局部治疗或局部治疗后出现进展,同时根治疗法也不适用 4.经研究者判断,既往未接受过任何全身治疗,且不愿意接受标准全身治疗疗法或不适合标准全身治疗疗法 5.ECOG体能状态评分 ≤ 1,肝功能为Child-Pugh A级
主要排除标准:
1.已知患脑转移瘤或软脑膜转移瘤 2.患活动性自身免疫性疾病或具有可能复发的自身免疫性疾病病史 3.研究药物首次给药前 ≤ 2年的任何活动性恶性肿瘤,但不包括本研究所评价的特定癌症以及任何已治愈的局部复发型癌症 4.研究药物首次给药前 ≤ 14天,需使用皮质类固醇(泼尼松或等效药物 > 10 mg/天)或其他免疫抑制药物进行全身治疗的任何疾病 5.已知存在人类免疫缺陷病毒(HIV)感染病史
主要研究中心所在地(具体启动情况以后期咨询为准):
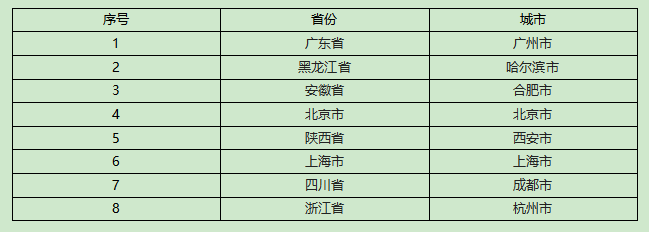
联系方式:
如果您身边有合适的患者欢迎与我们联系。24小时服务热线:400-001-2811

参与临床试验,不仅可以使用最新的治疗方法,医生还会密切关注您的病情状况。病情严重的患者,现行疗法效果不佳或者无力承担费用,参加临床试验免费尝试新的治疗方法,不管是对患者本人还是家属都是一种不错的选择。欢迎大家踊跃报名。注:最终能否入选需要由研究医生判定。
注:文章信息来源于网络,仅供医护人员内部讨论,不作为用药依据,具体用药指引,请咨询主治医师。
