



2019年12月21日,美国FDA宣布,加速批准第一三共(Daiichi Sankyo)和阿斯利康(AstraZeneca)共同开发,靶向HER2的抗体偶联药物(ADC)ENHERTU上市,治疗接受过2种或以上抗HER2疗法的治疗的无法切除或转移性HER2阳性乳腺癌患者。
英国阿斯利康公司(AstraZeneca)是全球领先制药公司,由前瑞典阿斯特拉公司和前英国捷利康公司于1999年合并而成。阿斯利康在6大治疗领域为患者提供富于创新,卓有成效的医药产品,包括消化、心血管、肿瘤、中枢神经、麻醉和呼吸等,其中许多产品居于世界领先地位。
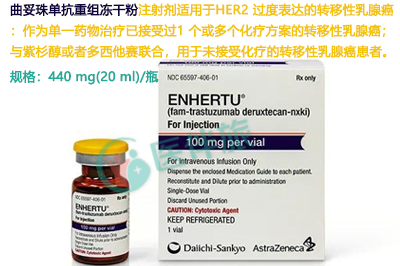
ENHERTU最常见的不良反应有:恶心(79%)、疲劳(59%)、呕吐(47%)、脱发(46%)、表明(35%)、食欲下降(32%)、贫血(31%)、腹泻(29%)、嗜中性白血球减少症(29%)、白血球减少症(22%)、白血球减少症(20%)、咳嗽(20%)、腹痛(19%)、头痛(19%)、上呼吸道感染(15%)……
ENHERTU最常见的3~4级不良反应有:嗜中性白血球减少症(16%)、恶心(7%)、贫血(7%)、疲劳(6%)、呕吐(3.8%)、低钾血症(3.4%)、白血球减少症(3.4%)、间质性肺病(2.6%)、腹泻(1.7%)、腹痛(1.3%)、食欲下降(1.3%)、呼吸困难(1.3%)……
ENHERTU最常见的实验室异常数据有:白细胞计数下降(70%)、血红蛋白减少(70%)、嗜中性粒细胞计数减少(62%)、天冬氨酸转氨酶增加(41%)、丙氨酸转氨酶增加(38%)、血小板减少(37%)、低钾血症(26%)。
ENHERTU最常见的3~4级实验室异常数据有:嗜中性粒细胞计数减少(16%)、白细胞计数下降(7%)、血红蛋白减少(7%)、血小板减少(3.4%)、低钾血症(3%)、天冬氨酸转氨酶增加(0.9%)、丙氨酸转氨酶增加(0.4%)。
相关热文推荐:英国阿斯利康Enhertu多少钱一瓶?/newsDetail/86020.html
注:文章信息来源于网络,仅供医护人员内部讨论,不作为用药依据,具体用药指引,请咨询主治医师。
